题目内容
下列各组离子在指定条件下,一定不能够大量共存的是( )
| A、滴加KSCN溶液后变成血红色的溶液中:K+、SO42-、Mg2+、H+ | ||
| B、由水电离出的c(H+)=1×10-13mol/L的溶液中:Fe2+、Na+、Mg2+、NO3-、Cl- | ||
C、
| ||
| D、能与Al反应产生H2的溶液:K+、Na+、Cl-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.滴加KSCN溶液后变成血红色的溶液,含Fe3+;
B.由水电离出的c(H+)=1×10-13mol/L的溶液,为酸或碱溶液;
C.
=0.1mol/L的溶液,显碱性;
D.能与Al反应产生H2的溶液,为非氧化性酸或强碱溶液.
B.由水电离出的c(H+)=1×10-13mol/L的溶液,为酸或碱溶液;
C.
| Kw |
| c(H+) |
D.能与Al反应产生H2的溶液,为非氧化性酸或强碱溶液.
解答:
解:A.滴加KSCN溶液后变成血红色的溶液,含Fe3+,该组离子之间不反应,可大量共存,故A不选;
B.由水电离出的c(H+)=1×10-13mol/L的溶液,为酸或碱溶液,碱溶液中不能存在Fe2+、Mg2+,酸溶液中Fe2+、H+、NO3-发生氧化还原反应,一定不能大量共存,故B选;
C.
=0.1mol/L的溶液,显碱性,该组离子之间不反应,可大量共存,故C不选;
D.能与Al反应产生H2的溶液,为非氧化性酸或强碱溶液,酸溶液中不生成氢气,碱溶液中该组离子之间不反应,可大量共存,故D不选;
故选B.
B.由水电离出的c(H+)=1×10-13mol/L的溶液,为酸或碱溶液,碱溶液中不能存在Fe2+、Mg2+,酸溶液中Fe2+、H+、NO3-发生氧化还原反应,一定不能大量共存,故B选;
C.
| Kw |
| c(H+) |
D.能与Al反应产生H2的溶液,为非氧化性酸或强碱溶液,酸溶液中不生成氢气,碱溶液中该组离子之间不反应,可大量共存,故D不选;
故选B.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
工业上用H2和N2直接合成氨:N2+3H2═2NH3,下列措施肯定能使合成氨反应速率加快的是( )
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④增大压强.
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④增大压强.
| A、只有①②③ | B、只有①②④ |
| C、只有①③④ | D、①②③④ |
乙醇分子中不同的化学键如图所示,对乙醇在各种反 应中应断裂的键说明不正确的是( )


| A、和钠作用键①断 |
| B、和浓H2SO4作用到170℃,键②和键⑤断 |
| C、和乙酸、浓H2SO4共热,键②断 |
| D、在Cu作用和O2反应,键①和键③断 |
下列实验装置设计正确的是( )
A、 干燥氢气 |
B、 稀释浓硫酸 |
C、 可移动铜丝符合绿色化学要求 |
D、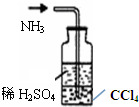 氨尾气吸收 |
 纽约一家公司设计出Soccket足球,每被踢一下,足球的内置机制就会把能量储存起来;被储存的能量可以通过USB接口给手机或其他小家电充电.在Soccket足球充放电的过程中,能量转化的主要形式是( )
纽约一家公司设计出Soccket足球,每被踢一下,足球的内置机制就会把能量储存起来;被储存的能量可以通过USB接口给手机或其他小家电充电.在Soccket足球充放电的过程中,能量转化的主要形式是( )| A、电能→化学能→电能 |
| B、化学能→电能→化学能 |
| C、机械能→电能→化学能 |
| D、机械能→化学能→电能 |
在Cu与稀HNO3的反应中,若有1mol HNO3被还原,则被氧化的Cu的物质的量为( )
A、
| ||
B、
| ||
| C、3mol | ||
D、
|
制造火箭的合金材料中的主要元素是( )
| A、Fe | B、Al | C、C | D、Si |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、室温下,42g乙烯和丙烯的混合气体中含有的碳原子数约为3NA |
| B、1mol C10H22分子中共价键总数为30NA |
| C、标准状况下,22.4 L四氯化碳的分子数为NA? |
| D、15g CH3+(碳正离子)中含有电子数为10NA |
 (1)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.写出FeCl3溶液腐蚀印刷电路铜板的离子方程式
(1)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等.写出FeCl3溶液腐蚀印刷电路铜板的离子方程式