题目内容
12.从能量的角度看,断开化学键要吸收能量、形成化学键要放出能量; 一个化学反应是释放能量还是吸收能量取决于反应物的总能量与生成物的总能量的相对大小.分析 根据断开化学键要吸收能量,形成化学键要放出能量;根据化学发应中能量变化的宏观表现回答.
解答 解:因断开化学键要吸收能量,形成化学键要放出能量,
一个化学反应是释放能量还是吸收能量取决于反应物的总能量与生成物的总能量的相对大小,若为放热反应,反应物总能量高于生成物总能量,若为吸热反应,应物总能量低于生成物总能量,
故答案为:吸收;放出;大小.
点评 本题主要考查了化学键的断开与形成与能量的关系、化学发应中能量变化的宏观表现,难度不大,根据课本知识即可完成.

练习册系列答案
相关题目
3.生活中的许多问题常涉及化学知识,它在给经济发展和群众生活带来方便的同时,也产生负面的影响.下列有关叙述正确的是( )
| A. | 次氯酸和臭氧都是强氧化剂,都能杀死水中的细菌.自来水常用氯气来杀菌消毒,是因为氯气杀菌消毒效果要比臭氧好,且不会残留有毒、有害物质 | |
| B. | 人们应用原电池原理,制成了多种电池,如干电池、充电电池、高能电池等.电池在现代生产和科学技术中发挥了重要作用,但废旧电池会对生态环境和公众健康造成危害,所以废旧电池必须回收再利用 | |
| C. | 明矾常用作净水剂,但人体摄入大量铝盐,易患老年性痴呆,所以明矾不宜大量作净水剂使用 | |
| D. | 氟氯烃为一类含有氟和氯的有机物,是制冷效果极佳的制冷剂,但它会破坏臭氧层,科研人员正在积极研发环保型的替代产品以减少氟氯烃的使用量 |
20.下列各组中的物质,在常温下能发生反应并产生气体的是( )
| A. | 铜与稀盐酸 | B. | 铁与浓硫酸 | C. | 铜与浓硝酸 | D. | 铜与稀硫酸 |
7.下列化合物中,含有共价键的离子化合物是( )
| A. | Na2S | B. | CaCl2 | C. | NaOH | D. | SO2 |
17.草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的性质,某化学研究性学习小组查阅了有关资料,有关物质的部分性质如表:
(1)为证明草酸受热分解的产物中含有CO2和CO(部分夹持仪器和加热装置省略),某课题小组设计实验如下:
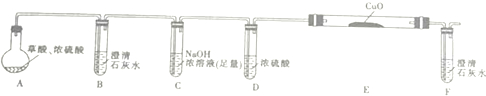
①写出E中反应的化学方程式并用双线桥标明电子转移的方向和数目: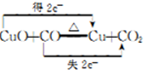
②用如图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,请你提出改进意见:在A与B之间添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管)
③利用改进后的装置进行实验时,要先加热A(填“A”“B”“C”“D”“E”或“F”,下同)装置,后加热E装置.
(2)该小组同学利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.实验时,先分别量 取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需的时间来判断反应的快慢.该小组设计了如下方案:
①已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4,为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4):n(KMnO4)≥2.5
②探究温度对化学反应速率影响的实验编号是Ⅱ和Ⅲ;探究反应物浓度对化学反应速率影响的实验编号是I和Ⅱ.
| 物质 | 熔点/℃ | 化学性质 |
| H2C2O4 | 189.5℃ | 二元弱酸,有毒,具有腐蚀性,易溶于水,100℃开始升华,157℃时开始分解,与浓硫酸混合加热会产生CO2、CO和H2O,草酸钙和草酸氢钙均为白色不溶物 |

①写出E中反应的化学方程式并用双线桥标明电子转移的方向和数目:

②用如图提供的仪器和试剂做实验时,装置B中出现白色浑浊,也不能说明一定有CO2,请你提出改进意见:在A与B之间添加一个盛水的洗气瓶,除去草酸蒸气(或在烧瓶上连接冷凝管)
③利用改进后的装置进行实验时,要先加热A(填“A”“B”“C”“D”“E”或“F”,下同)装置,后加热E装置.
(2)该小组同学利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.实验时,先分别量 取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需的时间来判断反应的快慢.该小组设计了如下方案:
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| Ⅰ | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| Ⅱ | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| Ⅲ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
②探究温度对化学反应速率影响的实验编号是Ⅱ和Ⅲ;探究反应物浓度对化学反应速率影响的实验编号是I和Ⅱ.
1.下列各组物质互为同分异构体的是( )
| A. | 12C和14C | B. | CH3-CH3和CH3-CH2-CH3 | ||
| C. | CH3-CH2-CH2-CH3和 | D. |  |
2.被称为“魔棒”的荧光棒已成为节日之夜青少年的喜爱之物,其发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光.已知草酸二酯的结构如图所示,下列有关说法正确的是( )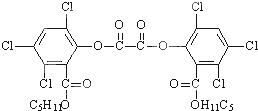

| A. | 1 mol草酸二酯与NaOH稀溶液反应(苯环上卤素不水解),最多可消耗10 mol NaOH | |
| B. | 草酸二酯水解时生成两种有机物 | |
| C. | 1 mol草酸二酯与H2完全反应,需要H2 6 mol | |
| D. | 草酸二酯的分子式为C26H22Cl6O8 |


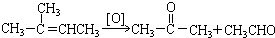
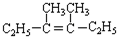 在上述类似条件下发生反应,请写出反应的方程式
在上述类似条件下发生反应,请写出反应的方程式 .
.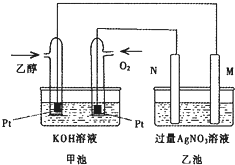 如图是个乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料分别是石墨和铁工作时M、N两个电极的质量都不减少,请回答:
如图是个乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料分别是石墨和铁工作时M、N两个电极的质量都不减少,请回答: