题目内容
【题目】反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,有关该反应的下列说法正确的是
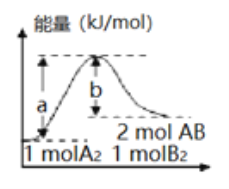
A. 每生成2 mol AB分子,需要吸收b kJ热量
B. 加入催化剂,(a-b)的差值减小
C. 该反应的反应物断键吸收的能量大于生成物成键放出的能量
D. 若反应生成AB为液态,每生成2 mol AB分子,需要吸收的热量大于(a-b) kJ
【答案】C
【解析】反应热=正反应活化能减去逆反应活化能;反应热=反应物断键吸收的能量减去生成物成键放出的能量;加入催化剂,改变反应历程,不能改变反应的反应热;气态物质变为液态要放出热量;据此分析解题。
根据图象分析判断1molA2和1molB2反应生成2molAB,每生成2molAB吸收(a-b) kJ热量,A错误;催化剂只能够降低反应的活化能,不能改变反应的反应热,(a-b)的差值不变,B错误;该反应为吸热反应,因此该反应的反应物断键吸收的能量大于生成物成键放出的能量,C正确;根据图象分析判断1molA2和1molB2反应生成2molAB,每生成2molAB(g)吸收(a-b) kJ热量,AB由气态变为液态,还要放出热量,因此若反应生成AB为液态,每生成2 mol AB分子,需要吸收的热量小于(a-b) kJ,D错误;正确选项C。

练习册系列答案
相关题目