题目内容
20.表是元素周期表的一部分.A、B、C、D均为短周期元素,若C原子最外层电子数是其内层电子总数的$\frac{3}{5}$,则下列说法中不正确的是( )| A | B | |
| C | D |
| A. | 阴离子半径从大到小的排列顺序为:C>D>B | |
| B. | B元素的两种同素异形体常温下都是气体 | |
| C. | 最高价氧化物对应的水化物的酸性:D>C | |
| D. | B元素的氢化物的沸点低于C元素的氢化物的沸点 |
分析 A、B、C、D均为短周期元素,若C原子最外层电子数是其内层电子总数的$\frac{3}{5}$,C为第三周期元素时内层电子总数为10,则最外层电子数为6,C为S元素;结合元素在周期表的位置可知,A为N,B为O,D为Cl,以此来解答.
解答 解:由上述分析可知,A为N,B为O,C为S,D为Cl,
A.电子层越多,离子半径越大,具有相同电子排布的离子中原子序数大的离子半径小,则阴离子半径从大到小的排列顺序为:C>D>B,故A正确;
B.B元素的两种同素异形体为氧气、臭氧,常温下都是气体,故B正确;
C.非金属性Cl>S,最高价氧化物对应的水化物的酸性:D>C,故C正确;
D.水分子间含氢键,则B元素的氢化物的沸点高于C元素的氢化物的沸点,故D错误;
故选D.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、原子结构、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
10.下列有机物命名正确的是( )
| A. |  2-乙基丙烷 | B. | CH3CH2CH2OH 1-丙醇 | ||
| C. |  间二甲苯 | D. |  2-甲基-2-丙烯 |
11.等物质的量的CO和CO2相比较,下列有关叙述中正确的是( )
①它们所含的分子数目之比为1:1 ②它们所含的O原子数目之比为1:2 ③它们所含的原子数目之比为2:3 ④它们所含的C原子数目之比为1:1 ⑤它们所含的电子数目之比为7:11.
①它们所含的分子数目之比为1:1 ②它们所含的O原子数目之比为1:2 ③它们所含的原子数目之比为2:3 ④它们所含的C原子数目之比为1:1 ⑤它们所含的电子数目之比为7:11.
| A. | ①②④ | B. | ①②③ | C. | ①②③⑤ | D. | 全部正确 |
8.下列现象不能用盐类水解知识解释的是( )
| A. | 泡沫灭火器利用Al3+、HCO3-相互反应可放出二氧化碳气体 | |
| B. | 使用热的纯碱水洗手时更容易除去手上的油脂污垢 | |
| C. | 明矾能用于净水 | |
| D. | 铜绿的生成 |
15.下列各组微粒具有相同的质子数和电子数的是( )
| A. | OH-、H2O、F- | B. | NH3、NH4+、NH2- | C. | H3O+、NH4+、NH2- | D. | HCl、F2、H2S |
5.下列化学用语书写正确的是( )
| A. | 甲烷的电子式: | B. | 丙烯的键线式: | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 苯的化学式:C8H8 |
12.下列有关离子化合物、共价化合物的性质描述,不正确的是( )
| A. | 离子化合物都能溶于水,而共价化合物都不溶于水 | |
| B. | 离子化合物的熔点一般较高,而共价化合物的熔点一般较低 | |
| C. | 离子化合物的硬度一般较大,而共价化合物的硬度一般较小 | |
| D. | 离子化合物在熔融条件下能够导电,而共价化合物在熔融条件下不能导电 |
9.化学与航空、航天密切相关,下列说法错误的是( )
| A. | 镁用于制造轻合金,是制造飞机、火箭的重要材料 | |
| B. | 高纯度硅制成的光电池,可用作火星探测器的动力 | |
| C. | 聚脂纤维属于新型无机非金属材料,可制作宇航服 | |
| D. | 高温结构陶瓷耐高温、耐氧化,是喷气发动机的理想材料 |
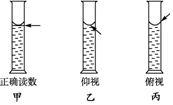 在配制一定物质的量浓度溶液的实验中,用量筒去取用一定量的浓溶液.量液时,量筒必须放平,视线要跟量筒内液体的凹液面最低点保持水平(如图甲),再读出液体的体积数.
在配制一定物质的量浓度溶液的实验中,用量筒去取用一定量的浓溶液.量液时,量筒必须放平,视线要跟量筒内液体的凹液面最低点保持水平(如图甲),再读出液体的体积数.