题目内容
物质的量浓度相同的下列溶液中.符合按PH由小到大顺序排列的是( )
| A、HCl NH4Cl CH3COOH NaNO3 Na2CO3 NaHCO3 NaOH |
| B、HCl NH4Cl CH3COOH NaHCO3 NaNO3 Na2CO3 NaOH |
| C、HCl CH3COOH NH4Cl NaNO3 NaHCO3 Na2CO3 NaOH |
| D、HCl CH3COOH NH4Cl NaNO3 Na2CO3 NaHCO3 NaOH |
考点:溶液pH的定义,盐类水解的应用
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:根据“谁强谁显性、谁弱谁水解”确定溶液酸碱性,从而确定溶液pH大小,注意碳酸根离子水解能力大于碳酸氢根离子.
解答:
解:碳酸氢钠和碳酸钠都是强碱弱酸盐,其溶液呈碱性,氢氧化钠是强碱,硝酸钠是强酸强碱盐,其溶液呈中性,氯化铵是强酸弱碱盐其溶液呈酸性,HCl是强酸,CH3COOH是弱酸,但碳酸氢根离子水解能力小于碳酸根离子,相同浓度时水解能力越大其碱性越强,所以pH从小到大顺序是HCl<CH3COOH<NH4Cl<NaNO3<NaHCO3<Na2CO3<NaOH;
故选C.
故选C.
点评:本题考查了溶液pH大小的平衡,先将盐根据其相应酸碱的强弱分类,再根据弱根离子的水解程度分类,从而比较pH相对大小,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质叙述不属于蛋白质变性的是( )
| A、蛋白质溶液加入食盐变浑浊 |
| B、用福尔马林溶液侵泡动物标本 |
| C、打针时用医用酒精消毒 |
| D、动物的皮经过药剂鞣制后,变成柔软坚韧的皮革 |
有人设想将不溶的碳酸盐材料通过特殊的加工方法使之变为纳米碳酸盐材料(即碳酸盐材料粒子直径是纳米级),这将使建筑材料的性能发生巨大变化,下列关于纳米碳酸盐材料的推测正确的是( )
| A、纳米碳酸盐材料是与胶体相似的分散系 |
| B、纳米碳酸盐材料分散到水中会产生丁达尔效应 |
| C、纳米碳酸盐材料的化学性质已与原来的碳酸盐材料完全不同 |
| D、纳米碳酸盐材料的粒子不能透过滤纸 |
电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH--2e-═ZnO+H2O Ag2O+H2O+2e-═2Ag+2OH-,下列判断正确的是( )
| A、锌为正极,Ag2O为负极 |
| B、锌为负极,发生还原反应 |
| C、原电池工作时,负极区溶液pH减小 |
| D、原电池工作时,负极区溶液pH增大 |
下列有机分子中,所有的原子不可能处于同一平面的是( )
| A、CH2═CHCN |
| B、CH2═CH-CH═CH2 |
| C、苯乙烯 |
| D、异戊二烯 |
下列过程或现象与盐类水解无关的是( )
| A、纯碱溶液去油污 |
| B、水中加入明矾可以净化水 |
| C、加热稀醋酸溶液其pH 稍有减小 |
| D、实验室配置FeCl3溶液时,加入少量HCl,以防止溶液浑浊 |
利用下列实验装置完成相应的实验,不能达到实验目的是( )
A、 验溶液中是否含有Na+ |
B、 提取溴水中的溴 |
C、 向容量瓶中转移液体 |
D、 除去CO气体中的CO2气体 |
下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是( )
①H2O ②NH3 ③Cl- ④CN- ⑤CO.
①H2O ②NH3 ③Cl- ④CN- ⑤CO.
| A、①② | B、①②③ |
| C、①②④ | D、①②③④⑤ |
2012年白酒行业塑化剂风波成为人们关注的焦点,塑化剂的其中一种邻苯二甲酸二丁酯(DBP)的结构如图所示,可由邻苯二甲酸(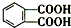 )与正丁醇发生酯化反应制得,下列有关说法不正确的是( )
)与正丁醇发生酯化反应制得,下列有关说法不正确的是( )
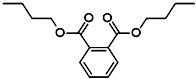
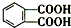 )与正丁醇发生酯化反应制得,下列有关说法不正确的是( )
)与正丁醇发生酯化反应制得,下列有关说法不正确的是( )
| A、邻苯二甲酸二丁酯(DBP)分子式为:C16H22O4 |
| B、邻苯二甲酸二丁酯(DBP)苯环上的一氯代物有2种 |
| C、邻苯二甲酸二丁酯(DBP)属于苯的同系物 |
| D、丁醇有4种不同结构,正丁醇是其中的一种,分子式为C4H10O |