题目内容
硝酸工厂的尾气氮氧化合物若不加以处理排放到大气中,不仅会形成硝酸型酸雨,还可以形成光化学烟雾.因此必须对含有氮氧化合物的废气进行处理.
(1)用氢氧化钠溶液可以吸收废气中的氮氧化合物,反应的化学方程式为:NO2+NO+2NaOH═2NaNO2+H2O
标出电子转移的方向和数目.在该反应中,每生成1mol NaNO2转移电子的数目为 .
(2)汽车尾气中含有NO和CO,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成N2和CO2.该反应的化学方程式为 :氧化剂是 ,还原剂是 .
(1)用氢氧化钠溶液可以吸收废气中的氮氧化合物,反应的化学方程式为:NO2+NO+2NaOH═2NaNO2+H2O
标出电子转移的方向和数目.在该反应中,每生成1mol NaNO2转移电子的数目为
(2)汽车尾气中含有NO和CO,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成N2和CO2.该反应的化学方程式为
考点:氮的氧化物的性质及其对环境的影响,氧化还原反应
专题:元素及其化合物
分析:(1)依据化学方程式中元素化合价的变化分析,标注电子转移,结合电子转移总数计算,反应NO2+NO+2NaOH═2NaNO2+H2O中,只有N元素化合价发生变化;
(2)一氧化氮和一氧化碳在催化剂条件下反应生成二氧化碳和氮气,元素化合价升高的做还原剂,元素化合价降低的做氧化剂;
(2)一氧化氮和一氧化碳在催化剂条件下反应生成二氧化碳和氮气,元素化合价升高的做还原剂,元素化合价降低的做氧化剂;
解答:
解:(1)反应NO2+NO+2NaOH═2NaNO2+H2O中,NO2中N元素化合价由+4价降低为NaNO2中的+3价,NO2是氧化剂;
NO中N元素化合价由+2价降低为NaNO2中的+3价,NO是还原剂,电子转移为: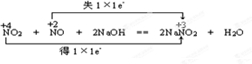 ;生成2molNaNO2,电子转移
;生成2molNaNO2,电子转移
1mol电子,生成1molNaNO2,电子转移0.5mol即0.5NA,故答案为: ,0.5NA;
,0.5NA;
(2)一氧化氮和一氧化碳经过排气管中的催化转化器转化为对大气无污染的物质,应生成氮气、二氧化碳,反应方程式为:2NO+2CO
N2+2CO2,反应中氧化剂为NO,还原剂为CO;
故答案为:2NO+2CO
N2+2CO2,NO,CO;
NO中N元素化合价由+2价降低为NaNO2中的+3价,NO是还原剂,电子转移为:
 ;生成2molNaNO2,电子转移
;生成2molNaNO2,电子转移1mol电子,生成1molNaNO2,电子转移0.5mol即0.5NA,故答案为:
 ,0.5NA;
,0.5NA;(2)一氧化氮和一氧化碳经过排气管中的催化转化器转化为对大气无污染的物质,应生成氮气、二氧化碳,反应方程式为:2NO+2CO
| ||
故答案为:2NO+2CO
| ||
点评:本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,为高频考点,注意从元素化合价的角度认识相关概念,结合反应的化学方程式计算,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列与化学概念有关的说法正确的是( )
| A、水玻璃、漂白粉、液氯均为混合物 |
| B、含有共价键的物质中一定不含有金属元素 |
| C、有单质参加或生成的化学反应一定是氧化还原反应 |
| D、35Cl与37Cl核外电子排布相同,化学性质相同 |
一定温度下,在密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法不正确的是( )
| 物质 | X | Y | Z | W |
| 初始浓度/mol?L-1 | 0.5 | 0.5 | 0 | 0 |
| 平衡浓度/mol?L-1 | 0.1 | 0.1 | 0.4 | 0.4 |
| A、反应达到平衡时,X的体积分数为10% |
| B、该温度下反应的平衡常数K=16 |
| C、保持温度不变增大压强,反应速率加快,平衡向正反应方向移动 |
| D、若X、Y的初始浓度均为0.8 mol?L-1,相同条件下达到平衡,W的浓度为0.64 mol?L-1 |
将11.2g的Mg-Cu混合物完全溶解于足量的硝酸中,收集反应产生x的气体.在向所得溶液中加入足量的NaOH溶液,产生21.4g沉淀.根据题意推断气体x的成分可能是( )
| A、0.3molNO2和0.3molNO |
| B、0.2molNO2和0.1molN2O4 |
| C、0.1molNO、0.2molNO2和0.05molN2O4 |
| D、0.6molNO |
下列仪器:①蒸馏烧瓶 ②普通漏斗 ③分液漏斗 ④蒸发皿 ⑤燃烧匙 ⑥量筒 ⑦天平中,常用于物质分离的是( )
| A、①②③④ | B、①③⑤⑥ |
| C、①③④⑥ | D、②③④⑦ |
欲萃取碘水中的碘,下列物质能作为萃取剂的是( )
| A、汽油 | B、盐酸 |
| C、酒精 | D、氢氧化钠溶液 |
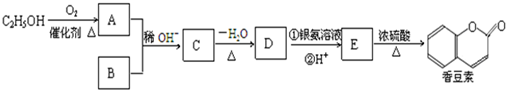
 (R、R′为烃基)
(R、R′为烃基)