题目内容
7.已知短周期元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )| A. | 质子数c>b | B. | 离子的还原性Z->Y2- | ||
| C. | 氢化物的稳定性H2Y>HZ | D. | 原子半径X>W |
分析 离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,则有a-3=b-1=c+2=d+1,可知原子序数a>b>d>c,Y、Z为非金属,处于第二周期,故Y为O元素,Z为F元素,W、X为金属处于第三周期,W为Al元素,X为Na元素,结合元素周期律解答.
解答 解:离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,则有a-3=b-1=c+2=d+1,可知原子序数a>b>d>c,Y、Z为非金属,处于第二周期,故Y为O元素,Z为F元素,W、X为金属处于第三周期,W为Al元素,X为Na元素.
A.由以上分析可知c=8,b=11,则质子数c<b,故A错误;
B.非金属性F>O,非金属性越强,对应的单质的氧化性越强,则阴离子的还原性越弱,则离子还原性Y2->Z-,故B错误;
C.非金属性F>O,非金属性越强氢化物越稳定性,氢化物稳定性为HZ>H2Y,故C错误;
D.W为Al元素,X为Na元素,原子半径Na>Al,故D正确,
故选D.
点评 本题考查结构与位置关系、元素周期律等,难度中等,根据电荷与核外电子排布相同推断元素在周期表中的位置是关键.

练习册系列答案
相关题目
14.下列各组物质中,所含分子数相同的是( )
| A. | 10g H2 和10g O2 | B. | 5.6lL N2(标准状况下)和11gCO2 | ||
| C. | 9克H2O和0.5mol 02 | D. | 224mL H2(标准状况下)和0.1mol N2 |
15.下列四组实验,根据实验事实得出的结论,正确的是( )
| A. | 在某未知试液中加入浓的NaOH溶液并加热,产生能使湿润的蓝色石蕊试纸变红的气体--原未知试液中一定含有NH4+ | |
| B. | 在某未知试液中加入硝酸银溶液,产生白色沉淀--原未知试液中一定含有Cl- | |
| C. | 用洁净的铂丝蘸取某溶液,置于火焰上灼烧,观察到火焰呈黄色--原溶液中一定含有Na+,不含有K+ | |
| D. | 在某未知试液中滴加过量的稀盐酸得到澄清溶液,再往澄清溶液中加入BaCl2溶液得白色沉淀--原未知试液中一定含有SO42- |
12. (1)用轨道示意图表示Fe3+的价电子排布
(1)用轨道示意图表示Fe3+的价电子排布 .
.
(2)某主族元素的电离能(电子伏特)如下:
,判断该元素处于VA族;
(3)若ABn的中心原子A上没有未用于形成共价键的孤对电子,运用价层电子对互斥模型,下列说法正确的是C(填字母).
A.若n=2,则分子的立体构型为V形
B.若n=3,则分子的立体构型为三角锥形
C.若n=4,则分子的立体构型为正四面体形
D.以上说法都不正确
(4)臭氧分子的结构如图1,呈V型,键角116.5°.请回答:
①臭氧与氧气的关系是同素异形体.
②下列分子与臭氧分子的结构最相似的是C(填字母).
A.H2O B.CO2 C.SO2 D.BeCl2
③臭氧分子是否为极性分子是(填“是”或“否”).
(5)在短周期元素中,由三种元素组成的既有离子键又有共价键和配位键,且阴、阳离子所含电子数相差8个,该物质的电子式 .
.
(6)金属钛为六方最密堆积结构,测得钛的原子半径为r,晶胞结构如图2所示,求该晶胞的边长a=2r,b=$\frac{4\sqrt{6}}{3}$r(用含r的代数式表示)
 (1)用轨道示意图表示Fe3+的价电子排布
(1)用轨道示意图表示Fe3+的价电子排布 .
.(2)某主族元素的电离能(电子伏特)如下:
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 14.5 | 29.6 | 47.4 | 77.5 | 97.9 | 551.9 | 666.8 |
(3)若ABn的中心原子A上没有未用于形成共价键的孤对电子,运用价层电子对互斥模型,下列说法正确的是C(填字母).
A.若n=2,则分子的立体构型为V形
B.若n=3,则分子的立体构型为三角锥形
C.若n=4,则分子的立体构型为正四面体形
D.以上说法都不正确
(4)臭氧分子的结构如图1,呈V型,键角116.5°.请回答:
①臭氧与氧气的关系是同素异形体.
②下列分子与臭氧分子的结构最相似的是C(填字母).
A.H2O B.CO2 C.SO2 D.BeCl2
③臭氧分子是否为极性分子是(填“是”或“否”).
(5)在短周期元素中,由三种元素组成的既有离子键又有共价键和配位键,且阴、阳离子所含电子数相差8个,该物质的电子式
 .
.(6)金属钛为六方最密堆积结构,测得钛的原子半径为r,晶胞结构如图2所示,求该晶胞的边长a=2r,b=$\frac{4\sqrt{6}}{3}$r(用含r的代数式表示)
19.推理是一种重要的学习和研究方法.下列推理正确的是( )
| A. | 单质中只含一种元素,所以只含一种元素的物质一定是单质 | |
| B. | 化学变化前后物质的质量总和不变,所以1g H2和1g O2一定能够生成2g H2O | |
| C. | 碱性溶液能使酚酞溶液变红,所以能使酚酞溶液变红的物质一定呈碱性 | |
| D. | 中和反应有盐和水生成,所以有盐和水生的反应一定是中和反应 |
17.如表是反应的离子方程式,其中评价关系不正确的是( )
| 选项 | 反应 | 离子方程式 | 评价 |
| A | 亚硫酸钡与盐酸反应 | BaSO3+2H+═Ba2++SO2↑+H2O | 正确 |
| B B | 向NaHSO4溶液中逐滴加入Ba(OH)2至溶液呈中性 | H++SO42-+Ba2++OH-═BaSO4+H2O | 正确 |
| C C | 铝制易拉罐去膜后放入NaOH溶液中 | 2Al+2OH-═2AlO2-+H2↑ | 错误,方程式未配平 |
| D | 少量铁粉与稀硝酸反应 | 3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | 错误,少量铁粉与稀硝酸反应应生成Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
 在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值可以确定有机物分子中氢原子的种类和数目
在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值可以确定有机物分子中氢原子的种类和数目

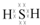 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多原子半径增大,得电子能力逐渐减弱.
;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多原子半径增大,得电子能力逐渐减弱.