题目内容
下列物质里含氢原子数最多的是:( )
| A、1 mol H2 |
| B、0.5molNH3 |
| C、6.02×1023个的CH4分子 |
| D、0.3molH3PO4 |
考点:物质的量的相关计算
专题:
分析:根据n=
结合物质的分子构成计算.
| N |
| NA |
解答:
解:由n=
可知,氢原子的物质的量越多,原子个数越多,
A.1 mol H2含有2molH;
B.0.5molNH3含有1.5molH;
C.6.02×1023个的CH4的物质的量为1mol,含有4molH;
D.0.3molH3PO4含有0.9mol,
则氢原子个数最多的为C,
故选C.
| N |
| NA |
A.1 mol H2含有2molH;
B.0.5molNH3含有1.5molH;
C.6.02×1023个的CH4的物质的量为1mol,含有4molH;
D.0.3molH3PO4含有0.9mol,
则氢原子个数最多的为C,
故选C.
点评:本题考查物质的量的计算,为高频考点,侧重于学生的分析能力的考查,注意把握相关计算公式的运用,难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
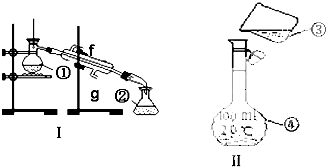
下列装置所示实验中,不能达到实验目的是( )
A、 制取少量氨气 |
B、 实验室制取氢氧化亚铁 |
C、 比较红磷和白磷的着火点 |
D、 实验室制取乙烯 |
为了证明液溴与苯发生的反应是取代反应,有如下图所示装置.则装置A中盛有的物质是( )


| A、水 |
| B、NaOH溶液 |
| C、CCl4 |
| D、NaI溶液 |
向100mL18mol/L的H2SO4溶液中加入足量的铜片并加热,充分反应,再加入足量的锌片,充分反应后,被还原的H2SO4的物质的量( )
| A、小于0.9mol |
| B、等于0.9mol |
| C、在0.9mol与1.8mol之间 |
| D、等于1.8mol |
NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、0.1mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 |
| B、2.8gN2和2.24 LCO组成的混合物中质子数为1.4 NA |
| C、将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,若不考虑挥发,溶液中一定含有NA个NH4+ |
| D、25℃时,1LpH=13的 Ba(OH)2溶液中含有的OH-数目为0.2 NA |
1mol/L的NaCl溶液表示( )
| A、溶液中含有1molNaCl |
| B、1L溶液里含有NaCl58.5克 |
| C、58.5gNaCl溶于941.5g水中 |
| D、1molNaCl溶于1L水中 |
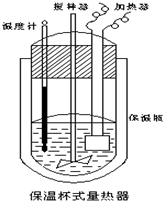 在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1.
在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1.