题目内容
20.用铝热法还原下列氧化物,制得金属各1mol,消耗铝最少的是( )| A. | MnO2 | B. | WO3 | C. | Fe2O3 | D. | V2O5 |
分析 根据化合价的变化判断,化合价变化的数值越小,说明发生氧化还原反应时得到的电子数目越少,则消耗铝的量最少,据此解答.
解答 解:MnO2~Mn,生成1molMn,需要4mol电子,消耗$\frac{4}{3}$molAl;
WO3~W,生成1molW,需要6mol电子,消耗2molAl;
Fe2O3~2Fe,生成1molFe,需要3mol电子,消耗1molAl;
V2O5~2V,生成1molV,需得电子5mol,消耗$\frac{5}{3}$molAl;
所以制得金属各1mol,消耗铝最少的是为C,
故选C.
点评 本题考查铝热反应,侧重于氧化还原反应的判断,明确反应中元素化合价变化是解题关键,题目不难.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
10.某元素的两种同位素,它们的原子具有不同的( )
| A. | 质子数 | B. | 质量数 | C. | 原子序数 | D. | 电子数 |
8.碳化硅的晶体有类似金刚石的结构,其中碳原子和硅原子的位置是交替的.它与晶体硅和金刚石相比较,正确的是( )
| A. | 熔点从高到低的顺序是:金刚石>碳化硅>晶体硅 | |
| B. | 熔点从高到低的顺序是:金刚石>晶体硅>碳化硅 | |
| C. | 三种晶体中的结构单元都是三角锥结构 | |
| D. | 三种晶体都是原子晶体且均为电的良导体 |
12.高中阶段我们相继学习了同位素、同素异形体、同分异构体、同系物的概念,下列有关这四个概念说法不正确的是( )
| A. | 因为C2H6与C3H8互称同系物,所以C4H8与C6H12一定互称同系物 | |
| B. | 氕、氘、氚互称同位素 | |
| C. | O2与O3、红磷与白磷、金刚石与石墨互称同素异形体 | |
| D. | 邻二甲苯、间二甲苯、对二甲苯互称同分异构体 |
9.已知W、X、Y、Z为短周期元素,它们的原子半径依次增大,W与Z、X和Y分别同主族,Y、Z同周期.X和Y能形成两种常见共价化合物,Z能与X形成两种常见的离子化合物,阴、阳离子个数比均为1:2.下列说法错误的是( )
| A. | Y、Z、X、W的原子序数依次减小 | |
| B. | X的简单氢化物的沸点低于Y的简单氢化物的沸点 | |
| C. | 由W、X、Y、Z四种元素组成的化合物可能显强酸性 | |
| D. | W和X形成的化合物,与W和Y形成的化合物中各元素质量比可能相同 |
10.一定温度下,反应 N2(g)+O2(g)?2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
| A. | 缩小体积使压强增大 | B. | 恒容,充入N2 | ||
| C. | 恒容,充入He | D. | 恒压,充入He |
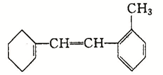
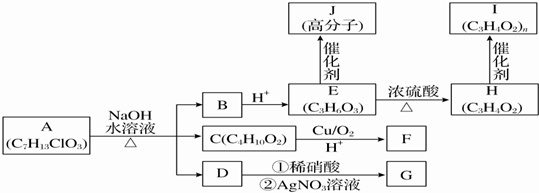
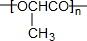 .
.