题目内容
【题目】高铁酸钾(K2FeO4)既能消毒杀菌,又能净水,是一种理想的水处理剂。工业 上制备高铁酸钾的一种工艺流程如下:
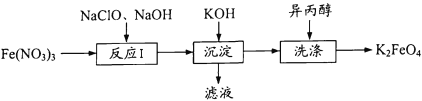
(1)K2FeO4中铁元素的化合价为 ____。
(2) “反应I”中参加反应的Fe3+与ClO-的物质的量之比为2 : 3,则滤液中含氯物质的化学式为____。写出“反应I”的离子方程式:_____。
(3)K2FeO4在水中发生反应:4K2FeO4+ 10H2O = 4Fe(OH)3 (胶体)+8KOH+3O2 ↑。高铁酸钾能消毒杀菌是因为____;它能净水是因为_____。
【答案】+6 NaCl 2Fe3+ + 3ClO-+10OH-= 2FeO42-+3Cl-+5H2O 具有强氧化性 生成的Fe(OH)3胶体具有吸附作用,可以吸附水中的杂质
【解析】
有流程可知Fe(NO3)3在碱性条件下与NaClO发生氧化还原反应生成硝酸钠、高铁酸钠、氯化钠和水,向反应所得溶液中加入氢氧化钾,析出溶解度较小的K2FeO4,用异丙醇洗涤得到K2FeO4。
(1)由化合价代数和为零可知K2FeO4中铁元素的化合价为+6价,故答案为:+6;
(2)设滤液中含氯物质的化合价为x,由得失电子数目守恒可得(6—3)×2=(1—x)×3,解得x=—1,则滤液中含氯物质为NaCl,由此可知Fe(NO3)3在碱性条件下与NaClO发生氧化还原反应生成硝酸钠、高铁酸钠、氯化钠和水,反应的离子方程式为2Fe3+ + 3ClO-+10OH-= 2FeO42-+3Cl-+5H2O,故答案为:NaCl;2Fe3+ + 3ClO-+10OH-= 2FeO42-+3Cl-+5H2O;
(3)高铁酸钾具有强氧化性,能起到杀菌消毒的作用,杀菌消毒过程中高铁酸钾被还原生成的Fe(OH)3胶体具有吸附作用,可以吸附水中的杂质,可以达到净水的作用,故答案为:具有强氧化性;生成的Fe(OH)3胶体具有吸附作用,可以吸附水中的杂质。

 阅读快车系列答案
阅读快车系列答案【题目】以废铁屑(含有少量镍)制备高铁酸钾(K2FeO4)的流程如下图所示:
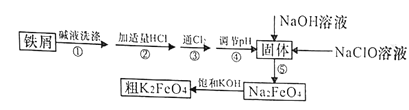
已知:25℃时,一些金属氢氧化物开始沉淀和完全沉淀时的pH如下表所示:
M(OH)m | PH | |
开始沉淀 | 沉淀完全 | |
Fe (OH)3 | 2.53 | 2.94 |
Ni(OH)2 | 7.60 | 9.75 |
(1)K2FeO4中铁元素的化合价为________________。
(2)“碱液洗涤”的目的是除去铁屑表面的油污,实际一般选用Na2CO3溶液除污,选用Na2CO3溶液除污的原理是____________________________(用离子方程式表示)。
(3)步骤③发生反应的离子方程式为___________________。
(4)步骤⑤是将Fe(OH)3固体氧化为Na2FeO4,同时NaClO转化为NaCl。则生成1mol Na2FeO4消耗NaClO的质量为______g;步骤④调节pH的范围是_______。
(5)用滴定法测定所制粗K2FeO4的纯度(杂质与KI不反应):取0.220g粗K2FeO4样品,加入足量硫酸酸化的KI溶液,充分反应后,用0.200mol·L-1Na2S2O3标准溶液滴定生成的I2,滴定消耗标准溶液的体积为20.00mL。涉及的反应有:FeO42-+4I-+8H+=Fe2++2I2+4H2O,2S2O32-+I2=S4O62-+2I-。
①滴定时选用的指示剂为______,滴定终点的现象为_____________。
②粗K2FeO4的纯度为_____________。
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为__(写离子符号);若所得溶液c(HCO3):c(CO32)=2:1,溶液pH=__。(室温下,H2CO3的K1=4×107;K2=5×1011)
(2)CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
已知上述反应中相关的化学键键能数据如下:
化学键 | C—H | C=O | H—H | C |
键能/kJ·mol1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=__。分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是__(填“A”或“B”)。
(3)向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①下列叙述能说明此反应达到平衡状态的是___。
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H-H键断裂
②产物甲醇可以用作燃料电池,碱性条件下的甲醇(CH3OH)燃料电池负极反应式:__。



