题目内容
14.我国最新报道的高温超导体中,铊(Ti)是组成的成分之一,已知铊与铝是同族元素,关于铊的性质的判断可能错误的是( )| A. | 是银白色、质软的金属 | |
| B. | 阳离子氧化性比铝离子强 | |
| C. | 加热蒸干TiCl3溶液可得到无水TiCl3 | |
| D. | 与稀硝酸作用生成硝酸盐 |
分析 铊与铝是同族元素,则具有金属的共性,化合物中元素的化合价为+3价,且金属性Tl>Al,以此来解答.
解答 解:A、铊与铝是同族元素,属于金属元素,则是银白色、质软的金属,故A正确;
B、同主族从上到下金属性在增强,则其阳离子的氧化性减弱,所以阳离子氧化性比铝离子弱,故B错误;
C、同主族从上到下金属性在增强,TiCl3在溶液中不水解,则加热蒸干TiCl3溶液可得到无水TiCl3,故C正确;
D、Tl较活泼,则该金属能与硝酸反应生成硝酸盐,故D正确;
故选B.
点评 本题考查同主族元素的性质,明确元素周期律是解答本题的关键,注意性质的相似性和递变性来解答即可,难度不大.

练习册系列答案
相关题目
4.短周期原子序数依次增大的主族元素R、T、Q、W、Y具有如下信息:①R、Y原子的最外层电子数与电子层数相同;②Q是地壳中含量最高的元素,R与T的核电荷数之和等于Q的核电荷数;③W与R同主族.下列说法正确的是( )
| A. | 元素Q与W形成的两种常见化合物中含有相同比例的阴、阳离子,与水反应产物不完全相同 | |
| B. | 元素T、Q、W、Y的原子半径大小为:T<Q<Y<W | |
| C. | Q与Y组成的常见物质是一种两性物质,结构中含有离子键 | |
| D. | 由Y和T组成的物质YT是,在电子和陶瓷工业上有广泛应用,可以直接由单质Y和T在低温下合成 |
5.下列关于苯酚的叙述中,错误的是( )
| A. | 其水溶液显强酸性,俗称石炭酸 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 碳酸氢钠溶液中滴入苯酚的水溶液后不会放出二氧化碳 |
2.已知H-H键能为436kJ•mol-1,N-H键能为391kJ•mol-1,根据化学方程式:N2+3H2 $\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$2NH3.1mol N2反应放出的热量 为92.4kJ•mol-1那么N≡N键的键能是( )
| A. | 431 kJ•mol-1 | B. | 945.6 kJ•mol-1 | C. | 649 kJ•mol-1 | D. | 896 kJ•mol-1 |
9.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | NaH2PO4水溶液呈酸性,其溶液中:c(Na+)>c(H2PO4-)>c(H3PO4)>c(HPO42-) | |
| B. | O.1 mol•L-1的CH3COONa溶液与0.1 mol•L-1的CH3COOH溶液等体积混合(PH<7):c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+) | |
| C. | O.1 mol•L-1的(NH4)2SO4溶液与O.1 mol•L-1的NH3•H2O溶液等体积混合:c(NH4+)+c(H+)=2c(SO42-)+c(OH-) | |
| D. | O.1 mol•L-1的Na2CO3溶液与O.2 mol•L-1的NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
19.某有机物W的分子式为C5H10O2能发生银镜反应,又能和钠反应产生气体.W的同分异构体有( )
| A. | 10种 | B. | 12种 | C. | 15种 | D. | 18种 |
6.某单官能团有机物的分子式为C3H6O,它可能的结构共有(不考虑立体异构)( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
13.如图是元素周期表的一部分,下列说法中,正确的是( )


| A. | 元素①位于第二周期第ⅣA族 | B. | 气态氢化物的稳定性:⑤>③ | ||
| C. | 元素的最高正化合价:④=② | D. | 最高价氧化物对应水化物酸性:⑤>④ |
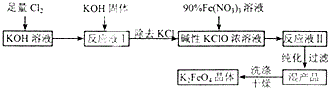 高铁酸钾(K2FeO4)是一种新型多功能水处理剂.其生产工艺如下:
高铁酸钾(K2FeO4)是一种新型多功能水处理剂.其生产工艺如下: