题目内容
15.如图是s能级和p能级的原子轨道图,试回答下列问题: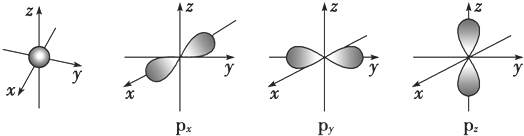
(1)s电子的原子轨道呈球形,每个s能级有1个原子轨道;p电子的原子轨道呈纺锤形,每个p能级有3个原子轨道.
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是2p电子,其电子云在空间有三个互相垂直的伸展方向;元素X的名称是氮,它的氢化物的电子式是
 .若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为S,原子的电子排布图为
.若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为S,原子的电子排布图为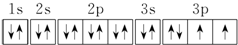 .
.
分析 (1)根据图片中轨道的形状进行分析解答,注意p能级有3个轨道;
(2)元素X的原子最外层电子排布式为nsnnpn+1,s能级最多排2个电子,该元素排列了p能级,说明s能级已经填满,所以n=2,则该元素最外层电子排布式为2s22p3,则该元素是N元素.
解答 解:(1)根据图片,s电子的原子轨道呈球形,含有1个原子轨道;p电子的原子轨道呈纺锤形,每个p能级有3个原子轨道,且这三个轨道相互垂直,
故答案为:球,1;纺锤,3;
(2)因为元素X的原子最外层电子排布式为nsnnn+1,np轨道已排上电子,说明ns轨道已排满电子,即n=2,则元素X的原子核外电子排布式为1s22s22p3,是氮元素,原子中能量最高的是2p电子,其电子云在空间有三个互相垂直的伸展方向,氢化物的电子式是 ;当元素X的原子最外层电子排布式为nsn-1npn+1时,有n-1=2,则n=3,则X元素的原子核外电子排布式为1s22s22p63s23p4,是硫元素,原子的电子排布图为
;当元素X的原子最外层电子排布式为nsn-1npn+1时,有n-1=2,则n=3,则X元素的原子核外电子排布式为1s22s22p63s23p4,是硫元素,原子的电子排布图为 ;故答案为:2p; 三个互相垂直的伸展; 氮;
;故答案为:2p; 三个互相垂直的伸展; 氮;  ;S;
;S; ;
;
点评 本题考查了原子核外电子排布及轨道伸展方向等知识点,正确推断元素是解本题关键,难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
12.下列说法中错误的是( )
| A. | 只要是甜的物质,都是糖类 | |
| B. | 单糖是不能发生水解的最简单的糖类 | |
| C. | 淀粉纤维素都是天然有机高分子化合物 | |
| D. | 蔗糖和麦芽糖均为二糖 |
13.下列物质不能发生消去反应的是( )
| A. | 溴乙烷 | B. | 2-甲基-1-丙醇 | ||
| C. | 2-丙醇 | D. | 2,2-二甲基-1-丙醇 |
3.甲醇是基本有机化工原料.甲醇及其可制得产品的沸点如下.
(1)在425℃、A12O3作催化剂,甲醇与氨气反应可以制得二甲胺.二甲胺显弱碱性,与盐酸反应生成(CH3)2NH2Cl,溶液中各离子浓度由大到小的顺序为c(Cl-)>c[(CH3)2NH2+]>c(H+)>c(OH-).
(2)甲醇合成二甲基甲酰胺的化学方程式为:2CH3OH+NH3+CO?(CH3)2NCHO+2H2O△H若该反应在常温下能自发进行,则△H<0 (填“>”、“<”或“=“).
(3)甲醇制甲醚的化学方程式为:2CH3OH?CH3OCH3+H2O△H.一定温度下,在三个体积均为1.0L 的恒容密闭容器中发生该反应.
①x/y=$\frac{1}{2}$.
②已知387℃时该反应的化学平衡常数K=4.若起始时向容器I中充入0.1mol CH3OH、
0,.15mol CH3OCH3和0.10mol H2O,则反应将向正(填“正”或“逆”)反应方向进行.
③容器Ⅱ中反应达到平衡后,若要进一步提高甲醚的产率,可以采取的措施为降温.
(4)以甲醇为主要原料,电化学合成碳酸二甲酯工作原理如图所示.
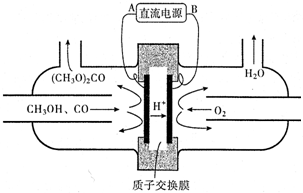
电源负极为B(填“A”或“B“),写出阳极的电极反应式2CH3OH+CO-2e-=(CH3O)2CO+2H+.
若参加反应的O2为1.12m3(标准状况),则制得碳酸二甲酯的质量为9.00kg.
| 名称 | 甲醇 | 二甲胺 | 二甲基甲酰胺 | 甲醚 | 碳酸二甲酯 |
| 结构式 | CH3OH | (CH3)2NH | (CH3)2NCHO | CH3OCH | (CH3O)2CO |
| 沸点(℃) | 64.7 | 7.4 | 153℃ | -24.9 | 90℃ |
(2)甲醇合成二甲基甲酰胺的化学方程式为:2CH3OH+NH3+CO?(CH3)2NCHO+2H2O△H若该反应在常温下能自发进行,则△H<0 (填“>”、“<”或“=“).
(3)甲醇制甲醚的化学方程式为:2CH3OH?CH3OCH3+H2O△H.一定温度下,在三个体积均为1.0L 的恒容密闭容器中发生该反应.
| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
| CH3OH | CH3OCH3 | H2O | ||
| Ⅰ | 387 | 0.20 | x | |
| Ⅱ | 387 | 0.40 | y | |
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
②已知387℃时该反应的化学平衡常数K=4.若起始时向容器I中充入0.1mol CH3OH、
0,.15mol CH3OCH3和0.10mol H2O,则反应将向正(填“正”或“逆”)反应方向进行.
③容器Ⅱ中反应达到平衡后,若要进一步提高甲醚的产率,可以采取的措施为降温.
(4)以甲醇为主要原料,电化学合成碳酸二甲酯工作原理如图所示.

电源负极为B(填“A”或“B“),写出阳极的电极反应式2CH3OH+CO-2e-=(CH3O)2CO+2H+.
若参加反应的O2为1.12m3(标准状况),则制得碳酸二甲酯的质量为9.00kg.
20.研究人员研制利用低品位软锰矿浆(主要成分是MnO2)吸收硫酸厂的尾气SO2,制备硫酸锰的生产流程如图1:
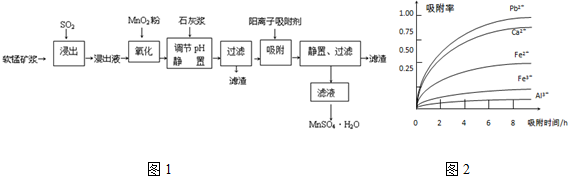
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子.PbO2的氧化性大于MnO2.有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见图2.
(1)浸出过程中生成Mn2+反应的化学方程式为SO2+MnO2=MnSO4,
(2)Fe2+被氧化的过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至4.7≤pH<8.3范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子半径、金属离子电荷等(写二点).
(5)吸附步骤除去的主要离子为Pb2+、Ca2+.
(6)电解MnSO4、ZnSO4和H4SO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式Mn2+-2e-+2H2O=MnO2↓+4H+.

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子.PbO2的氧化性大于MnO2.有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见图2.
| 离子 | 离子半径(pm) | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
(2)Fe2+被氧化的过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至4.7≤pH<8.3范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子半径、金属离子电荷等(写二点).
(5)吸附步骤除去的主要离子为Pb2+、Ca2+.
(6)电解MnSO4、ZnSO4和H4SO4的混合溶液可制备MnO2和Zn,写出阳极的电极反应方程式Mn2+-2e-+2H2O=MnO2↓+4H+.
4.过程一定有化学变化的是( )
| A. | 盐溶于水 | B. | 酒精挥发 | C. | 水结成冰 | D. | 铁器生锈 |
 如图所示,A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
如图所示,A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空: