题目内容
(每空2分,共12分)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4C1、FeC13、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是 (写化学式)。
(2)写出并配平该反应的化学方程式:
(3)发生氧化反应的物质是 ,反应中4mol的氧化剂能 (填“失去”或
“得到”) mol电子.
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为 。
(1)H2O;(2)6NH4C1+ 4Fe2O3→6Fe+2FeC13+3N2↑+12H2O;
(3)NH4C1 、得到、 24;(4)80g。
【解析】
试题分析:根据题意结合元素守恒可知X是H2O; (2)该反应的化学方程式是6NH4C1+ 4Fe2O3→6Fe+2FeC13+3N2↑+12H2O;(3)在该反应中发生氧化反应的物质是NH4C1中的N元素化合价升高,失去电子,被氧化,所以发生氧化反应的物质是NH4C1;在反应中每4mol的氧化剂Fe2O3发生还原反应,能够得到电子4×2×3=24mol;(4)根据方程式可知若产生3mol的N2,被还原的物质Fe2O3的物质的量是3mol,反应中被氧化产生了11.2LN2(标准状况)的气体时,n(N2)=0.5mol,被还原的物质Fe2O3的的物质的量是0.5mol,其质量为0.5mol×160g/mol=80g。
考点:考查氧化还原反应的概念、计算、方程式配平的知识。

练习册系列答案
相关题目
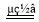 H2↑+ Cl2↑
H2↑+ Cl2↑ 3H++PO23-
3H++PO23-