题目内容
质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为 ( )
A.大于2c mol/L B.等于2c mol/L
C.小于2c mol/L D.在c mol/L-2c mol/L之间
A
【解析】
试题分析:令质量分数为a%KOH溶液的密度为xg/ml,质量分数为2a%KOH溶液的密度为yg/ml,则:
质量分数为a%KOH溶液的物质的量浓度为c=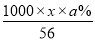 mol/L;
mol/L;
质量分数为2a%KOH溶液的物质的量浓度为c′=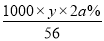 mol/L,
mol/L,
氢氧化钾溶液浓度越大密度越大,则x<y,故c′>2c。答案选A。
考点:考查物质的量的综合应用。

练习册系列答案
相关题目
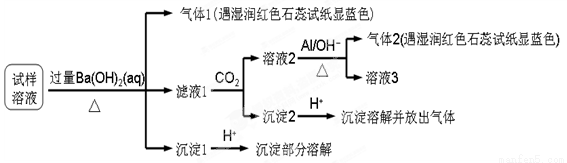
下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO | 稀硫酸 | 3Fe 2++NO |
B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-===Fe(OH)3↓ |
C | Ba2+、HCO | 氢氧化钠溶液 | HCO |
D | Al3+、Cl-、NO | 过量氢氧化钠溶液 | Al3++3OH-===Al(OH)3↓ |
 3NH3 + 8AlO2-
3NH3 + 8AlO2- 、K+
、K+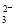 +H2O
+H2O