题目内容
13.下列说法正确的是( )| A. | 常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在:K+、Na+、AlO2-、SO42- | |
| B. | 向1 mo1•L-l CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高 | |
| C. | 25℃时,将a mo1•L-l氨水与0.01 moI•L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),用含a的代数式表示反应完全时NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ | |
| D. | 已知298K时,MgCO3的Ksp=6.82×10-6,溶液中c(Mg2+)=0.0001 mol•L-1,c(CO32-)=0.0001 mol•L-1,此时Mg2+和CO32-不能共存 |
分析 A.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,说明水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,偏铝酸根粒子与氢离子反应;
B.加入醋酸钠后,醋酸根离子浓度增大,导致醋酸的电离程度减小,溶液的pH增大;
C.当溶液中c(NH4+)=c(C1-),说明溶液呈中性,有c(H+)=c(OH-)=10-7,根据NH3•H2O的电离平衡常数的表达式进行计算;
D.如果溶液中c(Mg2+)•c(CO32-)<Ksp=6.82×10-6,则二者能共存,否则不能共存.
解答 解:A.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,说明水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,AlO2-与酸性溶液中的氢离子反应,在溶液中不能大量共存,故A错误;
B.CH3COO-的增加,抑制了CH3COOH的电离,导致溶液中c(H+)减小,则溶液的pH升高,故B错误;
C.当溶液中c(NH4+)=c(C1-),说明溶液呈中性,有c(H+)=c(OH-)=10-7,故NH3•H2O的电离平衡常数Kb=$\frac{0.005×1{0}^{-7}}{0.5(a-0.01)}$=$\frac{1{0}^{-9}}{a-0.01}$,故C正确;
D.c(Mg2+)•c(CO32-)=(0.0001)2=1×10-8<6.82×10-6,所以此时Mg2+和CO32-能共存,故D错误;
故选C.
点评 本题考查较综合,涉及难溶物的溶解平衡、弱电解质的电离、离子共存的判断等知识,题目难度中等,根据溶度积常数与浓度积之间的关系、弱电解质的电离特点、离子反应发生条件进行分析解答,B为易错点,需要明确溶液pH增大的根本原因.

练习册系列答案
相关题目
9.2015年4月28日,著名物理化学家徐光宪与世长辞,他在稀土萃取领域有惊人的成就,被誉为“稀土界的袁隆平”,稀土元素铈(Ce),其金属单质在空气中易氧化;加热时,在空气中燃烧;能溶于酸,不溶于碱;常见的化合价为+3和+4,氧化性Ce4+>Fe3+.下列说法不正确的是( )
| A. | 铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑ | |
| B. | 四种铈的核素${\;}_{58}^{136}$Ce、${\;}_{58}^{138}$Ce、${\;}_{58}^{142}$Ce,它们互为同位素 | |
| C. | 用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+ | |
| D. | 金属铈应储存于阴凉、通风的地方,包装要密封,不可与空气接触 |
4.某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物,当参加反应的单质与被还原HNO3的物质的量之比为2:1时,还原产物可能是( )
| A. | N2O | B. | NO | C. | NO2 | D. | N2 |
8.常温下,0.1mol•L-1某一元酸(HA)溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-8,相同物质的量浓度的某一元碱(BOH)溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×1012,下列叙述正确的是( )
| A. | HA的pH=3;BOH的pH=13 | |
| B. | pH=a的HA溶液,稀释10倍,其pH=a+1 | |
| C. | 等体积的HA和BOH恰好完全反应,溶液的pH=7 | |
| D. | 相同体积相同pH的HA和盐酸分别与足量Zn反应,生成氢气的物质的量相同 |
18.制取CH3CH2Cl,采用的最佳方法是( )
| A. | 乙烷和氯气取代反应 | B. | 乙烯和氯气加成反应 | ||
| C. | 乙烯和HCl加成反应 | D. | 乙烷和HCl作用 |
2.下列说法正确的是( )
| A. | 决定有机物种类繁多的原因是组成有机物的元素种类较多 | |
| B. | C5H12有四种同分异构体 | |
| C. |  用系统命名法命名:3,4,4-三甲基-6-乙基庚烷 用系统命名法命名:3,4,4-三甲基-6-乙基庚烷 | |
| D. |  与 与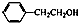 互为同系物 互为同系物 |
3.化学家借助太阳能产生的电能和热能,用空气和水作原料合成了氨气.下列有关说法正确的是( )
| A. | 该合成中所有的电能和热能全部转化为化学能 | |
| B. | 该合成氨过程不属于氮的固定 | |
| C. | 空气、水、太阳能均为可再生资源 | |
| D. | 断裂N2中的N≡N键会释放出能量 |
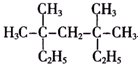 3,3,5,5-四甲基庚烷.
3,3,5,5-四甲基庚烷. .
. .
.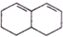 与Br2发生1,4-加成反应的化学方程式为
与Br2发生1,4-加成反应的化学方程式为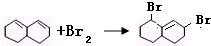 .
.