题目内容
【题目】常温下,将一定浓度的HA和HB分别与0.10mol/L的NaOH溶液等体积混合,实验记录如下表:
实验编号 | 加入的酸 | 加入酸的浓度/(mol/L) | 混合后溶液的pH |
① | HA | 0.10 | 8.7 |
② | HB | 0.12 | 2 |
下列说法中正确的是
A. HA是强酸,HB是弱酸
B. 升高温度,溶液②中c(B-)/c(Na+)增大
C. 溶液①中离子浓度的关系:c(A-)>c(Na+)>c(OH->c(H+)
D. 溶液②中离子浓度的关系:c(Na+)+c(H++c(B-)=0.12 mol/L
【答案】D
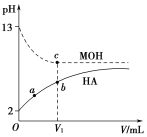
【解析】0.10mol/L的HA与0.10molL-1的NaOH溶液等体积混合,恰好完全反应生成NaA,溶液的pH=8.7,显碱性,说明NaA为强碱弱酸盐,即HA为弱酸;0.12mol/L的HB与0.10molL-1的NaOH溶液等体积混合,反应后剩余的酸的浓度为c(HB)=![]() =0.01mol/L,溶液中c(H+)=0.01mol/L,所以HB完全电离,即HB为强酸。A.由分析可知,HA是弱酸,HB是强酸,故A错误;B.NaB强酸强酸碱盐,升高温度,B-、Na+的浓度不变,所以溶液②中c(B-)/c(Na+)不变,故B错误;C.溶液①中,恰好完全反应生成NaA,溶液的pH=8.7,显碱性,c(OH-)>c(H+),水解程度较小,所以c(A-)>c(OH-),则离子浓度的关系:c(Na+)>c(A-)>c(OH-)>c(H+),故C错误;D.溶液②中c(H+)=0.01mol/l,c(B-)=0.12 molL-1×
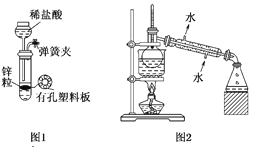
=0.01mol/L,溶液中c(H+)=0.01mol/L,所以HB完全电离,即HB为强酸。A.由分析可知,HA是弱酸,HB是强酸,故A错误;B.NaB强酸强酸碱盐,升高温度,B-、Na+的浓度不变,所以溶液②中c(B-)/c(Na+)不变,故B错误;C.溶液①中,恰好完全反应生成NaA,溶液的pH=8.7,显碱性,c(OH-)>c(H+),水解程度较小,所以c(A-)>c(OH-),则离子浓度的关系:c(Na+)>c(A-)>c(OH-)>c(H+),故C错误;D.溶液②中c(H+)=0.01mol/l,c(B-)=0.12 molL-1×![]() =0.06mol/L,c(Na+)=0.1mol/L×
=0.06mol/L,c(Na+)=0.1mol/L×![]() =0.05mol/L,所以c(Na+)+c(H+)+c(B-)=0.12 molL-1,故D正确;故选D。
=0.05mol/L,所以c(Na+)+c(H+)+c(B-)=0.12 molL-1,故D正确;故选D。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目