题目内容
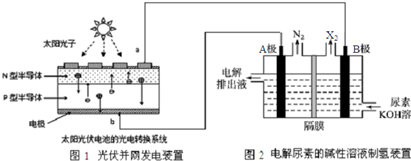
截至到2013年12月末,中国光伏发电新增装机容量达到10.66GW,光伏发电累计装机容量达到17.16GW,图1为光伏并网发电装置.图2为电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极).下列叙述中正确的是( )

| A、图1中N型半导体为正极,P型半导体为负极 |
| B、图2溶液中电子流向:从B极流向A极 |
| C、X2为氧气 |
| D、工作时,A极的电极反应式为CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该电池反应时中,氮元素化合价由-3价变为0价,H元素化合价由+1价变为0价,所以生成氮气的电极A是阳极,生成氢气的电极B是阴极,结合电解池的工作原理分析解答.
解答:
解:A.该电池反应时中,氮元素化合价由-3价变为0价,H元素化合价由+1价变为0价,则氮元素被氧化,氢元素被还原,所以生成氮气的电极A是阳极,生成氢气的电极B是阴极,则图1中N型半导体为负极,P型半导体为正极,故A错误;
B.电解时,电子的流向为:阳极→电源,电源→阴极,故B错误;
C.阴极B上水得电子生成氢气和氢氧根离子,电极反应式为2H2O+2e-═H2↑+2OH-,故C错误;
D.A极为阳极,电极反应式为:CO(NH2)2+80H--6e-═CO32-+N2↑+6H2O,故D正确;
故选:D.
B.电解时,电子的流向为:阳极→电源,电源→阴极,故B错误;
C.阴极B上水得电子生成氢气和氢氧根离子,电极反应式为2H2O+2e-═H2↑+2OH-,故C错误;
D.A极为阳极,电极反应式为:CO(NH2)2+80H--6e-═CO32-+N2↑+6H2O,故D正确;
故选:D.
点评:本题考查了电解原理,明确元素化合价变化与阴阳极的关系是解本题关键,根据电解池的工作原理来分析解答,难度中等.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
水体污染物有:I含盐酸的酸性废水,II悬浮颗粒,III重金属离子;污水处理的化学方法有:a中和法,b沉淀法,c混凝法.所采用的方法对水体污染物处理不正确的是( )
| A、I-a | B、I-b |
| C、II-c | D、III-b |
下列化合物的组成中,一定含有氢元素,但不一定含有氧元素的是( )
①碱
②酸
③酸性氧化物
④碱式盐
⑤酸式盐
⑥铵盐
⑦结晶水合物.
①碱
②酸
③酸性氧化物
④碱式盐
⑤酸式盐
⑥铵盐
⑦结晶水合物.
| A、只有①④⑦ | B、只有②⑥ |
| C、只有②⑤⑥ | D、只有③⑦ |
用铁片和稀硫酸反应制取氢气时,下列措施不能使氢气的生成速率加快的是( )
| A、加热 |
| B、将稀硫酸改为98%的浓硫酸 |
| C、将铁片改为铁粉 |
| D、将0.5mol?L-1的稀硫酸改为2mol?L-1的稀硫酸 |
下列物质中不能使淀粉碘化钾试纸变蓝色的是( )
| A、溴水 | B、食盐水 |
| C、新制氯水 | D、碘水 |
下列实验装置设计正确的是( )
A、 干燥氯气 |
B、 稀释浓硫酸 |
C、 可移动铜丝符合绿色化学要求 |
D、 氨尾气吸收 |
一定条件下,将0.1L CO、0.2L CO2、0.1L NO、0.2L NO2和0.2L NH3混合,然后通过分别盛有足量蒸馏水、饱和碳酸氢钠溶液和氢氧化钠溶液的三个洗气瓶(洗气瓶排列顺序不确定).假设气体通过每个洗气瓶都能充分反应,则尾气(已干燥)( )
| A、可能是单一气体 |
| B、不可能含有一氧化氮 |
| C、不可能存在原气体中的两种气体 |
| D、成分和洗气瓶的排列顺序无关 |
下列能用勒夏特列原理解释的事实是( )
| A、NaOH溶液使酯水解比稀H2SO4使酯水解更快 |
| B、由2NO2(g)?N2O4(g)组成的平衡体系,加压后颜色加深 |
| C、在硫酸亚铁溶液中,加入铁粉以防止氧化变质 |
| D、用热的纯碱溶液洗去铁屑表面的油污时,去污效果好 |