题目内容
用铁片和稀硫酸反应制取氢气时,下列措施不能使氢气的生成速率加快的是( )
| A、加热 |
| B、将稀硫酸改为98%的浓硫酸 |
| C、将铁片改为铁粉 |
| D、将0.5mol?L-1的稀硫酸改为2mol?L-1的稀硫酸 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:A、温度升高,化学反应速率增大;
B、一般增大反应物的浓度增大,反应速率增大,但应考虑浓硫酸的强氧化性来分析;
C、利用增大接触面积来分析加快反应速率;
D、增大反应物的浓度增大,反应速率增大.
B、一般增大反应物的浓度增大,反应速率增大,但应考虑浓硫酸的强氧化性来分析;
C、利用增大接触面积来分析加快反应速率;
D、增大反应物的浓度增大,反应速率增大.
解答:
解:A、因加热时反应体系的温度升高,则化学反应速率加快,故A错误;
B、因浓硫酸具有强氧化性,铁与浓硫酸反应生成二氧化硫而不生成氢气,故B正确;
C、改用铁粉,增大了铁与硫酸反应的接触面积,则反应速率加快,故C错误;
D、0.5mol?L-1的稀硫酸改为2mol?L-1的稀硫酸,即增大反应物酸的浓度,反应速率增大,故D错误.
故选B.
B、因浓硫酸具有强氧化性,铁与浓硫酸反应生成二氧化硫而不生成氢气,故B正确;
C、改用铁粉,增大了铁与硫酸反应的接触面积,则反应速率加快,故C错误;
D、0.5mol?L-1的稀硫酸改为2mol?L-1的稀硫酸,即增大反应物酸的浓度,反应速率增大,故D错误.
故选B.
点评:本题较简单,考查影响化学反应速率的常见因素,学生应熟悉温度、浓度、构成原电池、增大接触面等对化学反应速率的影响来解答,但浓硫酸的性质是学生解答中容易忽略的知识.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
下列物质分类正确的是( )
| A、波尔多液、工业酒精、氨水均为混合物 |
| B、稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C、烧碱、冰醋酸、四氯化碳均为电解质 |
| D、SO2、SiO2、CO均为酸性氧化物 |
随着科技的进步,研究和制备物质的手段和途径越来越多,C60、H3、O2+、N5+等已被发现.下列有关说法正确的是( )
| A、H2和H3属于同位素 |
| B、O2+中不含化学键 |
| C、C60中含有共价键 |
| D、N5+中含有离子键 |
下列仪器不能用酒精灯直接加热的是( )
| A、蒸馏烧瓶 | B、蒸发皿 |
| C、坩埚 | D、试管 |
截至到2013年12月末,中国光伏发电新增装机容量达到10.66GW,光伏发电累计装机容量达到17.16GW,图1为光伏并网发电装置.图2为电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极).下列叙述中正确的是( )
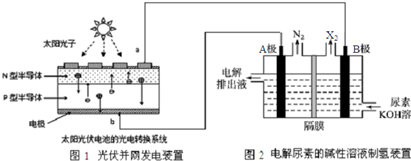

| A、图1中N型半导体为正极,P型半导体为负极 |
| B、图2溶液中电子流向:从B极流向A极 |
| C、X2为氧气 |
| D、工作时,A极的电极反应式为CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O |
下列有关能量的说法不正确的是( )
| A、化石能源物质内部贮存着大量的能量 |
| B、植物的光合作用使太阳能转化为化学能 |
| C、由石墨制金刚石是吸热反应,故石墨能量比金刚石能量低 |
| D、燃料燃烧时只是将化学能转化为热能 |
对于敞口容器中的化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g),下列叙述不正确的是( )
| A、锌不能用来表示该反应的速率,其它反应物和生成物都能用来表示该反应的速率(molL-1S-1) |
B、反应过程中能量关系可用如图表示 |
| C、若将该反应设计成原电池,锌为负极 |
| D、若将其设计为原电池,当有32.5g锌溶解时,正极放出11.2L气体 |
已知合成氨反应的浓度数据如下:
当用氢气浓度的减少来表示该化学反应速率时,其速率为( )
| N2+3H2?2NH3 | |||
| 起始浓度mol/L | 1.0 | 3.0 | 0 |
| 2秒末浓度mol/L | 0.6 | 1.8 | 0.8 |
| A、0.2mol/(L?s) |
| B、12mol/(L?min) |
| C、0.6mol/(L?s) |
| D、36mol/(L?min) |