题目内容
20.已知R元素的最高正化合价与最低负价的绝对值差为4,R原子最外层上的电子数是K层上电子数的3倍.则R元素的名称为( )| A. | 硫 | B. | 碳 | C. | 氮 | D. | 硅 |
分析 R原子最外层上的电子数是K层上电子数的3倍,最外层电子数为6,R元素的最高正化合价与最低负价的绝对值差为4,则最高正化合价为+6、最大负化合价为-2,结合选项进行判断.
解答 解:R原子最外层上的电子数是K层上电子数的3倍,最外层电子数为6,处于ⅥA族,R元素的最高正化合价与最低负价的绝对值差为4,则最高正化合价为+6、最大负化合价为-2,故选项中S元素符合,故选A.
点评 本题考查原子结构与元素性质,比较基础,注意理解化合价与族、最外层电子数关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构.下列说法正确的是( )
| A. | 原子最外层电子数:X>Y>Z | B. | 原子序数:X>Y>Z | ||
| C. | 单质沸点:Z>Y>X | D. | 离子半径:X2->Y+>Z- |
5.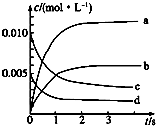 在2L密闭容器内,800℃时反应2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如下表:
(1)如图表示NO2的浓度变化的曲线是b.用O2表示从0~2s内该反应的平衡速率v=1.5×10-3mol•L-1•s-1.
(2)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变.
 在2L密闭容器内,800℃时反应2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变.
9.用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是( )
①加盐酸溶解 ②加入过量烧碱溶液 ③过滤 ④通入过量CO2生成Al(OH)3 沉淀⑤加入盐酸生成Al(OH)3沉淀.
①加盐酸溶解 ②加入过量烧碱溶液 ③过滤 ④通入过量CO2生成Al(OH)3 沉淀⑤加入盐酸生成Al(OH)3沉淀.
| A. | ①②⑤③ | B. | ②③④③ | C. | ②③⑤③ | D. | ①③⑤③ |
10.根据能量变化示意图,确定下列选项中正确的是( )
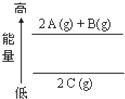

| A. | 2A(g)+B(g)=2 C(g)△H<0 | B. | 2A(g)+B(g)=2 C(g)△H>0 | C. | 2C(g)=2A(g)+B(g)△H>0 | D. | 2C(g)=2 A(g)+B(g)△H<0 |
 .
. .
.
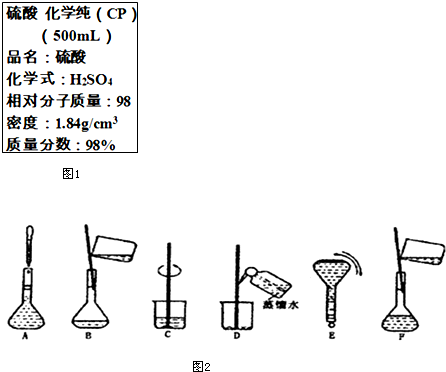 如图1是硫酸试剂瓶标签上的部分内容.现实验室需要240ml 4.6mol/L的稀硫酸用该硫酸配置,
如图1是硫酸试剂瓶标签上的部分内容.现实验室需要240ml 4.6mol/L的稀硫酸用该硫酸配置, Na2S
Na2S
 CO2
CO2 .
.