题目内容
11.写出下列反应的平衡常数表达式:C(s)+H2O(g)?H2(g)+CO(g) K=$\frac{c({H}_{2})c(CO)}{c({H}_{2}O)}$
2SO2(g)+O2?2SO3(g) K1=$\frac{{c}^{2}(S{O}_{3})}{c({O}_{2}){c}^{2}(S{O}_{2})}$
SO2(g)+$\frac{1}{2}$O2?SO3(g) K2=$\frac{c(S{O}_{3})}{c(S{O}_{2}){c}^{\frac{1}{2}}({O}_{2})}$
上述K1与K2的关系式为K1=K22.
分析 根据平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积,书写平衡常数,固体物质的浓度看作1,据此答题.
解答 解:平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积,
反应①C(s)+H2O(g)?CO(g)+H2(g)平衡常数K=$\frac{c({H}_{2})c(CO)}{c({H}_{2}O)}$,
反应②2SO2(g)+O2?2SO3(g) 平衡常数K1=$\frac{{c}^{2}(S{O}_{3})}{c({O}_{2}){c}^{2}(S{O}_{2})}$,
反应③SO2(g)+$\frac{1}{2}$O2?SO3(g) 平衡常数K2=$\frac{c(S{O}_{3})}{c(S{O}_{2}){c}^{\frac{1}{2}}({O}_{2})}$,
反应②×$\frac{1}{2}$=反应③,所以K1=K22,
故答案为:$\frac{c({H}_{2})c(CO)}{c({H}_{2}O)}$;$\frac{{c}^{2}(S{O}_{3})}{c({O}_{2}){c}^{2}(S{O}_{2})}$;$\frac{c(S{O}_{3})}{c(S{O}_{2}){c}^{\frac{1}{2}}({O}_{2})}$;K1=K22.
点评 本题考查化学平衡常数的意义,和平衡常数的书写、及综合应用,难度不大.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
19.某金属M的氯化物MCl2的相对分子质量为a,溶解度为Sg,现取质量为Wg的MCl2,在一定温度下完全溶解配成V mL饱和溶液,若溶液的密度为d g/cm3,溶液的物质的量浓度为c mol/L,溶液中溶质的质量分数为ω%,则下列关系式中不正确的是( )
| A. | c=$\frac{1000W}{aV}$mol/L | B. | c(Cl-)=$\frac{10dW}{a}$mol/L | C. | ω%=$\frac{100W}{dV}$% | D. | S=$\frac{100W}{dV-W}$ |
2.将磷肥生产中形成的副产物石膏(CaSO4•2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义.以下是石膏转化为硫酸钾和氯化钙的某工艺流程示意图.

(1)在这个工艺中,有很多粒子都具有相同的电子数.
写出该工艺中具有相同电子数的四种粒子的化学式:NH3、H2O、NH4+、OH-、H3O+五种的任意四种.
(2)1919年由Langmuir提出了等电子体.原子数相同、电子数相同的粒子,互称为等电子体.A、B、C、D、E、F 是原子序数依次增大的6种位于元素周期表前20号的元素.B、C、D、E位于同周期.C是构成空气的主要元素.F与B、D都可形成XY2型离子化合物FB2、FD2,且都可与A2D(无色液体)反应放出气体.B22-与C2是等电子体,D22-与E2是等电子体.F原子的N层电子数与K层电子数相同.
①比较C、D、E对应的简单阴离子的半径(用离子符号表示)N3->O2->F-(由大到小);
②写出能证明D和E非金属性强弱的一个化学方程式2F2+2H2O=4HF+O2.
③由上述6种元素中的4种构成的离子化合物是(写出两种)NH4HCO3、(NH4)2CO3、Ca(HCO3)2、(CH3COO)2Ca其中两种,其中所含的化学键类型有离子键、共价键.
(3)①过滤Ⅱ所得滤液中大量含有的阳离子有哪些?请分别检验.(可不填满下表)
②写出此工艺的总反应方程式CaSO4•2H2O+2KCl+4H2O=K2SO4+CaCl2•6H2O.

(1)在这个工艺中,有很多粒子都具有相同的电子数.
写出该工艺中具有相同电子数的四种粒子的化学式:NH3、H2O、NH4+、OH-、H3O+五种的任意四种.
(2)1919年由Langmuir提出了等电子体.原子数相同、电子数相同的粒子,互称为等电子体.A、B、C、D、E、F 是原子序数依次增大的6种位于元素周期表前20号的元素.B、C、D、E位于同周期.C是构成空气的主要元素.F与B、D都可形成XY2型离子化合物FB2、FD2,且都可与A2D(无色液体)反应放出气体.B22-与C2是等电子体,D22-与E2是等电子体.F原子的N层电子数与K层电子数相同.
①比较C、D、E对应的简单阴离子的半径(用离子符号表示)N3->O2->F-(由大到小);
②写出能证明D和E非金属性强弱的一个化学方程式2F2+2H2O=4HF+O2.
③由上述6种元素中的4种构成的离子化合物是(写出两种)NH4HCO3、(NH4)2CO3、Ca(HCO3)2、(CH3COO)2Ca其中两种,其中所含的化学键类型有离子键、共价键.
(3)①过滤Ⅱ所得滤液中大量含有的阳离子有哪些?请分别检验.(可不填满下表)
| 所含离子 | 检验方法 |
| K+ | 取少量滤液于试管中,通过焰色反应,火焰呈紫色(透过蓝色钴玻璃) |
| NH4+ | 取少量滤液于试管中,并向其中加入NaOH微热,有刺激性气味产生(该气体可使湿润红色石蕊试纸变蓝) |
3.已知金刚石和石墨在氧气中完全燃烧的热化学方程式如下:①C(金刚石,s)+O2(g)=CO2(g)△H1=-395.41kJ/mol;②C(石墨,s)+O2(g)=CO2(g)△H2=-393.51kJ/mol.关于金刚石与石墨的转化,下列说法正确的是( )
| A. | 金刚石转化成石墨是自发进行的过程 | |
| B. | 石墨转化成金刚石是自发进行的过程 | |
| C. | 石墨和金刚石能量一样高 | |
| D. | 金刚石比石墨能量低 |

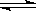 3C(g)+2D(s) △H>0。达到平衡时生成
3C(g)+2D(s) △H>0。达到平衡时生成 了1.8 mol C。
了1.8 mol C。
