题目内容
将足量二氧化硫通入下列各溶液中,所含离子因发生氧化还原反应而不能大量共存的是( )
| A、Ba2+、Na+、NH4+、Br-、Cl- |
| B、K+、Na+、AlO2-、SO42 -、SiO32 - |
| C、Na+、HCO3-、SO32 -、CH3COO- |
| D、H+、Fe3+、Na+、NO3-、SO32 - |
考点:离子共存问题
专题:离子反应专题
分析:A.Ba2+、Na+、NH4+、Br-、Cl-之间不发生反应,通入二氧化硫也不反应;
B.通入二氧化硫后硅酸根离子、偏铝酸根反应,该反应不属于氧化还原反应;
C.通入二氧化硫后碳酸氢根离子、亚硫酸根离子、醋酸根离子反应,但不属于氧化还原反应;
D.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚硫酸根离子和二氧化硫.
B.通入二氧化硫后硅酸根离子、偏铝酸根反应,该反应不属于氧化还原反应;
C.通入二氧化硫后碳酸氢根离子、亚硫酸根离子、醋酸根离子反应,但不属于氧化还原反应;
D.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚硫酸根离子和二氧化硫.
解答:
解:A.Ba2+、Na+、NH4+、Br-、Cl-之间不反应,通入二氧化硫也不反应,在溶液中能够大量共存,故A错误;
B.AlO2-、SiO32-与通入的二氧化硫反应,但是该反应不属于氧化还原反应,故B错误;
C.HCO3-、SO32-、CH3COO-与通入的二氧化硫反应,但不属于氧化还原反应,故C错误;
D.二氧化硫溶于水生成H2SO3,其能被硝酸、铁离子氧化而不能大量共存,故D正确;
故选D.
B.AlO2-、SiO32-与通入的二氧化硫反应,但是该反应不属于氧化还原反应,故B错误;
C.HCO3-、SO32-、CH3COO-与通入的二氧化硫反应,但不属于氧化还原反应,故C错误;
D.二氧化硫溶于水生成H2SO3,其能被硝酸、铁离子氧化而不能大量共存,故D正确;
故选D.
点评:本题考查离子共存的判断,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的H+或OH-;溶液的具体反应条件,如“所含离子因发生氧化还原反应而不能大量共存”、“加入铝粉产生氢气”等.

练习册系列答案
相关题目
配制一定物质的量浓度的某溶液,下列情况会使配制结果偏高的是( )
| A、定容摇匀后发现液面低于刻度线,再加水至刻度线 |
| B、容量瓶中原来含有少量蒸馏水 |
| C、未洗涤烧杯和玻璃棒 |
| D、定容时俯视刻度线观察液面 |
在给定条件的水溶液中一定能大量共存的离子组是( )
| A、无色溶液中:K+、Cu2+、Na+、MnO4-、SO42- |
| B、水电离产生的c(H+)=1×10-12mol?L-1的溶液中:Mg2+、SO42-、NO3-、Cl- |
| C、加入Al能放出H2的溶液中:Mg2+、Na+、NO3-、Cl- |
| D、能使pH试纸变为蓝色的溶液中:S2-、Na+、SO32-、Cl- |
用下列实验装置完成对应的实验(部分仪器已省),能达到实验目的是( )
A、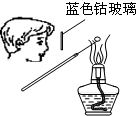 检验Na2CO3中的Na+ |
B、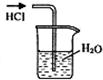 吸收HCl |
C、 石油的蒸馏 |
D、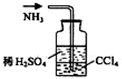 吸收NH3 |
关于下列各实验装置的叙述中,不正确的是( )

| A、图①可用于实验室制取少量NH3或O2 |
| B、可用从a处加水的方法检验图②装置的气密性 |
| C、实验室可用图③的方法收集Cl2或NH3 |
| D、利用图④装置制硫酸和氢氧化钠,其中b为阴离子交换膜、c为阳离子交换膜 |
下列有关物质应用的说法中,正确的是( )
| A、氢氧化铝具有弱碱性,可用于制胃酸中和剂 |
| B、用二氧化硫加工银耳,使之更白 |
| C、二氧化锰具有强氧化性,故能将双氧水氧化为氧气 |
| D、NH3极易溶于水,可用作制冷剂 |
 的系统命名为
的系统命名为 的分子式为
的分子式为