题目内容
14.下列关于物质的用途,叙述不正确的是( )| A. | Al(OH)3可作治疗胃酸过多的一种药剂 | |
| B. | 焰色反应为金属元素的物理性质 | |
| C. | 镁铝合金可用作制造飞机的材料 | |
| D. | 高纯硅用来制造光导纤维 |
分析 A.氢氧化铝为弱碱性,可以治疗胃酸过多;
B.焰色反应是金属原子中激发态电子跃迁到低能级时以光的形式释放能量;
C.镁铝合金硬度大、密度小;
D.二氧化硅用来制造光导纤维.
解答 解:A.胃酸主要成分为盐酸,氢氧化铝为弱碱性,中和过多的盐酸,可以治疗胃酸过多,故A正确;
B.焰色反应是金属原子中激发态电子跃迁到底能级时以光的形式释放能量,属于物理性质,故B正确;
C.镁铝合金硬度大、密度小,可用作制造飞机的材料;
D.二氧化硅用来制造光导纤维,高纯度硅用作半导体材料,故D错误.
故选:D.
点评 本题考查元素化合物性质与用途、焰色反应等,比较基础,主要对基础知识的理解掌握.

练习册系列答案
相关题目
4.下列实验事实解释不合理的是( )
| A. | 乙醇的沸点高于乙醛是因为乙醇分子间存在氢键,而乙醛分子间只有范德华力 | |
| B. | 单质碘易溶于CCl4而微溶于水,是因为I2和CCl4都是非极性分子而水是极性分子 | |
| C. | NH3与CH4的空间构型不同是因为NH3中存在孤电子对而CH4中只有成键电子对 | |
| D. | 水分子比硫化氢稳定是因为水分子存在氢键 |
5.下列离子方程式正确的是( )
| A. | 氯气与水反应:Cl2+H2O?2H++Cl-+ClO- | |
| B. | Ba(OH)2溶液与稀硫酸反应:Ba2++OHˉ+H++SO42-═BaSO4↓+H2O | |
| C. | CaCO3中加入稀盐酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | Mg(OH)2与盐酸反应:OHˉ+2H+═H2O |
9.在无色溶液中,下列各组离子能够大量共存的是( )
| A. | K+、Ba2+、Cl-、SO42- | B. | H+、HCO3-、Cl-、K+ | ||
| C. | Cl-、Na+、NO3-、Ca2+ | D. | Cu2+、NO3-、SO4-、Cl- |
19.下列物质中,属于电解质的是( )
| A. | 铜丝 | B. | MgCl2 | C. | 氨气 | D. | 蔗糖 |
6.下列各组物质中互为同位素的是( )
| A. | ${\;}_{6}^{12}$C和${\;}_{6}^{13}$C | B. | CH3CH2CH2CH3和CH3CHCH3CH3 | ||
| C. | 红磷和白磷 | D. | 甲烷和乙烷 |
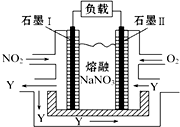 NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的负极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为NO2-e-+NO3-═N2O5.
NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨Ⅰ为电池的负极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为NO2-e-+NO3-═N2O5.