题目内容
4.下列实验事实解释不合理的是( )| A. | 乙醇的沸点高于乙醛是因为乙醇分子间存在氢键,而乙醛分子间只有范德华力 | |
| B. | 单质碘易溶于CCl4而微溶于水,是因为I2和CCl4都是非极性分子而水是极性分子 | |
| C. | NH3与CH4的空间构型不同是因为NH3中存在孤电子对而CH4中只有成键电子对 | |
| D. | 水分子比硫化氢稳定是因为水分子存在氢键 |
分析 A.乙醇分子间可形成氢键导致沸点较高;
B.一般说来,极性分子组成的溶质易溶于极性分子组成的溶剂,非极性分子组成的溶质易溶于非极性分子组成的溶剂;
C.CH4的中心原子没有孤电子对,其键角为109°28′,NH3的中心原子含有1个孤电子对,键角为107°18′;
D.分子稳定性与化学键有关,与氢键无关.
解答 解:A.乙醇分子间存在氢键,乙醛分子间不能形成氢键,所以乙醇的沸点比乙醛高,故A正确;
B.碘、CCl4是非极性分子,水是极性分子,根据物质溶解性“相似相溶”的一般规律,因此碘不易溶于水,易溶于CCl4,故B正确;
C.孤电子对与成键电子对间的斥力大于成键电子对间的斥力,CH4的中心原子没有孤电子对,其键角为109°28′,NH3的中心原子含有1个孤电子对,键角为107°18′,故C正确;
D.H2O分子比H2S分子稳定,是因H-O键能比H-S键能大,与氢键无关,故D错误;
故选D.
点评 本题考查了氢键、分子空间构型等知识,侧重氢键知识的综合应用考查,注意氢键不是化学键,分子稳定性与化学键有关,与氢键无关,为易错点,题目难度不大.

练习册系列答案
相关题目
14.下列有关化学用语表示正确的是( )
| A. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | B. | N2的电子式: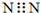 | ||
| C. | 硫离子结构示意图: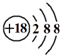 | D. | CH4分子的比例模型: |
15.表为元素周期表的一部分,用元素符号或化学用语回答下列问题.
(1)10种元素中,化学性质最不活泼的是Ar,除⑩外原子半径最大的是K
(2)①、②、④、⑧四种元素形成的离子半径由大到小的顺序为Cl->K+>Na+>Al3+,
(3)⑥和高价态的⑤形成的化合物的电子式是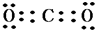 ,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为
,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为 ;用电子式表示元素③和⑨形成化合物的过程
;用电子式表示元素③和⑨形成化合物的过程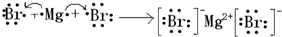
(4)⑥、⑦两种元素形成的简单氢化物中,沸点高的是H2O,原因是水分子之间存在氢键
(5)④和⑧两种元素最高价氧化物对应水化物相互反应的离子方程式3H++Al(OH)3=3H2O+Al3+
(6)写出一个能表示⑦、⑧两种元素非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓,
(7)下列叙述中,肯定a金属比b金属活泼性强的是D(填序号)
A.a原子的最外层电子数比b原子的最外层电子数少
B.a原子的电子层数比b原子的电子层数多
C.1mol a 从酸中置换H+生成的H2比1mol b从酸中置换H+生成的H2多
D.常温时,a能从水中置换出氢,而b不能.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑧ | ⑩ | ||
| 4 | ② | ⑨ |
(2)①、②、④、⑧四种元素形成的离子半径由大到小的顺序为Cl->K+>Na+>Al3+,
(3)⑥和高价态的⑤形成的化合物的电子式是
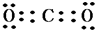 ,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为
,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为 ;用电子式表示元素③和⑨形成化合物的过程
;用电子式表示元素③和⑨形成化合物的过程
(4)⑥、⑦两种元素形成的简单氢化物中,沸点高的是H2O,原因是水分子之间存在氢键
(5)④和⑧两种元素最高价氧化物对应水化物相互反应的离子方程式3H++Al(OH)3=3H2O+Al3+
(6)写出一个能表示⑦、⑧两种元素非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓,
(7)下列叙述中,肯定a金属比b金属活泼性强的是D(填序号)
A.a原子的最外层电子数比b原子的最外层电子数少
B.a原子的电子层数比b原子的电子层数多
C.1mol a 从酸中置换H+生成的H2比1mol b从酸中置换H+生成的H2多
D.常温时,a能从水中置换出氢,而b不能.
12.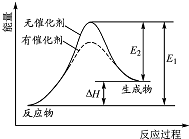 某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
 某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )| A. | 催化剂能改变该反应的焓变 | B. | 催化剂能降低该反应的活化能 | ||
| C. | 该反应为放热反应 | D. | E1 越大,表明该反应越容易发生 |
19.反应4X(g)+5Y(g)=4W(g)+6Q(g)在2L的密闭容器中进行,1分钟后,X 减少了0.12mol,则用Y来表示该反应在1分钟内的速率为( )
| A. | 0.06mol/(L•min) | B. | 0.075mol/(L•min) | C. | 0.09mol/(L•min) | D. | 0.12mol/(L•min) |
16.下列电离方程式正确的是( )
| A. | H2S?2H++S2- | B. | NaHSO4?Na ++HSO4- | ||
| C. | NaHCO3?Na++H++CO32- | D. | HCO3-+H2O?CO32-+H3O+ |
13.下表为六种短周期元素的部分性质,下列有关说法错误的是( )
| 元素代号 | X | Y | Z | Q | R | T |
| 原子半径/10-10m | 0.77 | 0.66 | 0.70 | 1.17 | 0.99 | 1.10 |
| 主要化合价 | +4、-4 | -2 | +5、-3 | +4、-4 | +7、-1 | +5、-3 |
| A. | X与Y可以形成阴离子XY32- | |
| B. | 元素R的氧化物对应水化物一定为强酸 | |
| C. | Z的氢化物的沸点比T的氢化物的沸点高 | |
| D. | 由X形成的化合物QX和XR4,其晶体类型不相同 |
14.下列关于物质的用途,叙述不正确的是( )
| A. | Al(OH)3可作治疗胃酸过多的一种药剂 | |
| B. | 焰色反应为金属元素的物理性质 | |
| C. | 镁铝合金可用作制造飞机的材料 | |
| D. | 高纯硅用来制造光导纤维 |