题目内容
 以图中A→K是中学化学中常见的物质,其中A、C、E是金属,F、G为气体单质,其余均为化合物,C焰色反应呈黄色,D为红棕色粉末,K为红褐色固体.
以图中A→K是中学化学中常见的物质,其中A、C、E是金属,F、G为气体单质,其余均为化合物,C焰色反应呈黄色,D为红棕色粉末,K为红褐色固体.请回答下列问题:
(1)写出K的化学式
(2)写出H的电子式
(3)反应①的化学方程式为
(4)反应②的离子方程式为
考点:无机物的推断
专题:推断题
分析:C为金属单质,焰色反应为黄色,则C为Na,C与水反应得到气体单质G与H溶液,则G为O2、H为NaOH;
D为红棕色粉末,为Fe2O3,与盐酸反应得到I为FeCl3,I与H(NaOH)反应得到红褐色固体K为Fe(OH)3,
金属单质E与H(NaOH)溶液反应得到J溶液与G(氢气),则E为Al、J为NaAlO2.E(Al)与D(氧化铁)反应得到金属A与B,则A为Fe,B为Al2O3,电解氧化铝得到Al与氧气,故B为O2,据此解答.
D为红棕色粉末,为Fe2O3,与盐酸反应得到I为FeCl3,I与H(NaOH)反应得到红褐色固体K为Fe(OH)3,
金属单质E与H(NaOH)溶液反应得到J溶液与G(氢气),则E为Al、J为NaAlO2.E(Al)与D(氧化铁)反应得到金属A与B,则A为Fe,B为Al2O3,电解氧化铝得到Al与氧气,故B为O2,据此解答.
解答:
解:C为金属单质,焰色反应为黄色,则C为Na,C与水反应得到气体单质G与H溶液,则G为O2、H为NaOH;
D为红棕色粉末,为Fe2O3,与盐酸反应得到I为FeCl3,I与H(NaOH)反应得到红褐色固体K为Fe(OH)3,
金属单质E与H(NaOH)溶液反应得到J溶液与G(氢气),则E为Al、J为NaAlO2.E(Al)与D(氧化铁)反应得到金属A与B,则A为Fe,B为Al2O3,电解氧化铝得到Al与氧气,故B为O2,
(1)由上述分析可知,K的化学式为:Fe(OH)3,故答案为:Fe(OH)3;
(2)H为NaOH,属于离子化合物,由钠离子与氢氧根离子构成,其电子式为: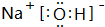 ,故答案为:
,故答案为: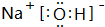 ;
;
(3)反应①是Al与氧化铁反应生成Fe与氧化铝,反应的化学方程式为:Fe2O3+2Al
2Fe+Al2O3,故答案为:Fe2O3+2Al
2Fe+Al2O3;
(4)反应②是Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
D为红棕色粉末,为Fe2O3,与盐酸反应得到I为FeCl3,I与H(NaOH)反应得到红褐色固体K为Fe(OH)3,
金属单质E与H(NaOH)溶液反应得到J溶液与G(氢气),则E为Al、J为NaAlO2.E(Al)与D(氧化铁)反应得到金属A与B,则A为Fe,B为Al2O3,电解氧化铝得到Al与氧气,故B为O2,
(1)由上述分析可知,K的化学式为:Fe(OH)3,故答案为:Fe(OH)3;
(2)H为NaOH,属于离子化合物,由钠离子与氢氧根离子构成,其电子式为:
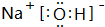 ,故答案为:
,故答案为: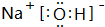 ;
;(3)反应①是Al与氧化铁反应生成Fe与氧化铝,反应的化学方程式为:Fe2O3+2Al
| ||
| ||
(4)反应②是Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评:本题以无机框图题的形式考查Na、Al、Fe等元素单质及化合物的相互转化关系,难度中等,C焰色反应呈黄色,D为红棕色粉末,K为红褐色固体等是解题突破口,再结合转化关系进行推断,对学生的逻辑推理能力提出较高的要求.

练习册系列答案
相关题目
下列反应属于吸热反应的是( )
| A、Ba(OH)2与HCl的中和反应 |
| B、葡萄糖在人体内氧化分解 |
| C、Ba(OH)2?8H20与NH4Cl反应 |
| D、锌粒与稀H2S04反应制取H2 |
已知反应:2H2O2=2H2O+O2↑,下列条件下,反应速率最大的是( )
| A、10℃,5mL 3%H2O2溶液 |
| B、10℃,5mL 5%H2O2溶液 |
| C、30℃,5mL 5%H2O2溶液 |
| D、30℃,5mL 5%H2O2溶液且加入少量MnO2 |
 如图是一些常见的单质和化合物之间的转化关系图,有些反应中的部分物质被略去.常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质.反应①、②均为工业上的重要反应.
如图是一些常见的单质和化合物之间的转化关系图,有些反应中的部分物质被略去.常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质.反应①、②均为工业上的重要反应. 两组同学对碳酸钠和碳酸氢钠的混合物与酸的反应进行探究.
两组同学对碳酸钠和碳酸氢钠的混合物与酸的反应进行探究.
