题目内容
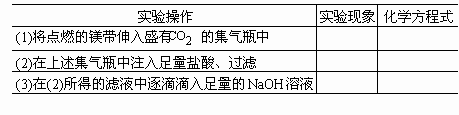
按下表所示实验,请填写空白.
解析:
|
镁带剧烈燃烧,集气瓶内壁附有白色、黑色粉末 2Mg+ 白色粉末逐渐溶解,过滤得黑色粉末和无色滤液 MgO+2HCl= 产生白色沉淀
|

 已知如表所示数据:
已知如表所示数据:| 物质 | 熔点(℃) | 沸点(℃) | 密度(g?cm-3) |
| 乙醇 | -117.3 | 78.5 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | - | 338.0 | 1.84 |
①在三颈烧瓶中按体积比2:3:3配制浓硫酸、乙醇和乙酸的混合液80mL.
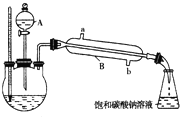
②按如图所示连接好装置(装置气密性良好,加热以及夹持装置省略),用小火均匀加热装有混合液的三颈烧瓶5~10min.
③边加热,边从仪器A向三颈烧瓶中滴加乙醇.
④待锥形瓶收集到一定量产物后停止加热,用力振荡锥形瓶,然后静置待分层.
⑤分离出乙酸乙酯层,洗涤、干燥.
请根据题目要求回答下列问题:
(1)仪器A使用前必须进行的操作是
(2)仪器B的名称是
(3)乙醇与乙酸反应的化学方程式是
(4)实验完成后,锥形瓶里液面上有透明的不溶于水的油状液体,若分离油状液体混合物,需要用到的主要玻璃仪器是
(5)用30g乙酸与46g乙醇反应,如果实际产量是理论产量的67%,则实际得到乙酸乙酯的质量是
A.44g B. 29.3g C.74.8g D.88g.
I.高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s) + 3CO(g) 2Fe(s)+3CO2(g)
△H
2Fe(s)+3CO2(g)
△H
(1)已知:①Fe2O3(s) + 3C(石墨)=2Fe(s) + 3CO(g) △H1
②C(石墨)+ CO2(g) = 2CO(g) △H2
则△H___________________(用含△H1 、△H2的代数式表示)。
(2)高炉炼铁反应的平衡常数表达式K=____________________________。
(3)在某温度时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
|
|
Fe2O3 |
CO |
Fe |
CO2 |
|
甲/mol |
1.0 |
1.0 |
1.0 |
1.0 |
|
乙/mol |
1.0 |
1.5 |
1.0 |
1.0 |
①甲容器中CO的平衡转化率为_______________________。
②下列说法正确的是____________________(填编号)。
A.若容器压强恒定,反应达到平衡状态
B.若容器内气体密度恒定,反应达到平衡状态
C.甲容器中CO的平衡转化率大于乙的
D.增加Fe2O3就能提高CO的转化率
II.纳米MgO可用尿素与氯化镁合成。某小组研究该反应在温度为378~398K时的反应时间、反应物配比等因素对其产率的影响。请完成以下实验设计表:
|
编号 |
温度/K |
反应时间/h |
反应物物质的量配比 |
实验目的 |
|
① |
378 |
4 |
3∶1 |
实验②和④探究________ ______________________ 实验②和__________探究 反应时间对产率的影响。 |
|
② |
378 |
4 |
4∶1 |
|
|
③ |
378 |
3 |
_______ |
|
|
④ |
398 |
4 |
4∶1 |
下图为温度对纳米MgO产率(曲线a)和粒径(曲线b)的影响,请归纳出温度对纳米MgO制备的影响规律(写出一条):
___________________________________________。

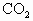
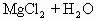
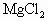 +2NaOH=Mg
+2NaOH=Mg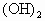 ↓+2NaCl
↓+2NaCl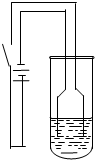 (2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
(2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究: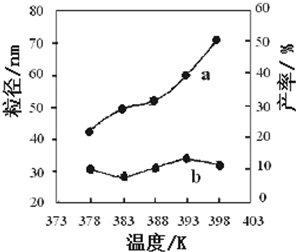 I.高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
I.高炉炼铁是冶炼铁的主要方法,发生的主要反应为: