题目内容
下列说法正确的是( )
| A、某原子的质量数为A,则该原子的相对原子质量也为A |
| B、稀有气体元素原子的最外层电子数均为8 |
| C、第二周期第ⅣA族元素的原子核电荷数和中子数一定为6 |
| D、原子序数为16的元素位于元素周期表的第三周期第ⅥA族 |
考点:质子数、中子数、核外电子数及其相互联系,原子结构与元素的性质
专题:原子组成与结构专题
分析:A.一种相对原子质量是这种原子的质量与C-12原子质量的
的比值;
B.He为2;
C.第二周期ⅣA族元素为碳元素,其质子数与中子数不一定相同;
D.原子序数为16的元素是硫元素.
| 1 |
| 12 |
B.He为2;
C.第二周期ⅣA族元素为碳元素,其质子数与中子数不一定相同;
D.原子序数为16的元素是硫元素.
解答:
解:A.质量数(A)=质子数(Z)+中子数(N),一种相对原子质量是这种原子的质量与C-12原子质量的
的比值,二者不相等,故A错误;
B.He为2,其他为8,故B错误;
C.第二周期ⅣA族元素为碳元素,其质子数与中子数不一定相同,如14C含有6个质子和8个中子,故C错误;
D.原子序数为16的元素是硫元素,位于第三周期第ⅥA族,故D正确.
故选D.
| 1 |
| 12 |
B.He为2,其他为8,故B错误;
C.第二周期ⅣA族元素为碳元素,其质子数与中子数不一定相同,如14C含有6个质子和8个中子,故C错误;
D.原子序数为16的元素是硫元素,位于第三周期第ⅥA族,故D正确.
故选D.
点评:本题考查质子数、中子数、核外电子数及其相互联系、结构与位置的关系、化合价与族序数的关系等,题目难度不大,掌握规律是解答的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
用氢氧化钠固体配制一定物质的量浓度的氢氧化钠溶液,下列情况使溶液浓度偏高的是( )
| A、所用氢氧化钠中混有氧化钠 |
| B、用托盘天平称取一定质量的氢氧化钠时,所用的小烧杯内壁不太干燥 |
| C、向容量瓶中加水超过刻度线 |
| D、最后确定氢氧化钠溶液的体积(定容)时,仰视观察容量瓶刻度线 |
下列实验操作或装置不能达到目的是( )
A、 稀释浓硫酸 |
B、 分液 |
C、 定容 |
D、 过滤 |
下列化学反应的产物不存在同分异构体的是( )
| A、2-丁醇在浓硫酸存在下发生脱水反应 |
| B、甲苯在铁粉存在下与液溴反应 |
| C、2-氯丙烷与NaOH醇溶液共热 |
| D、丙烯与氯化氢加成 |
下列反应的离子方程式正确的是( )
| A、Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
| B、用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O |
| C、Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| D、氨水与醋酸反应:NH3?H2O+CH3COOH?CH3COO-+NH4++H2O |
 下表各组物质中,按如图所示关系转化,不是所有反应都一步能实现的选项是( )
下表各组物质中,按如图所示关系转化,不是所有反应都一步能实现的选项是( )| 选项 | X | Y | Z |
| A | NO | NO2 | HNO3 |
| B | NaCl | NaOH | NaHCO3 |
| C | Al | NaAlO2 | Al(OH)3 |
| D | C | CO | CO2 |
| A、A | B、B | C、C | D、D |
对于反应 2H2(g)+O2(g)?2H2O(g);△H=-483.6kJ/mol,下列说法正确的是( )
| A、反应物具有的总能量高于生成物 |
| B、H2的燃烧热△H=-241.8kJ/mol |
| C、破坏H-H键要放出热量 |
| D、升高温度重新达到平衡,平衡常数增大 |
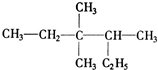 系统命名法命名为
系统命名法命名为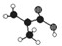 所示(图中球与球之间的连线代表化学键,如单键、双键等).
所示(图中球与球之间的连线代表化学键,如单键、双键等).