题目内容
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中不正确的是
| A.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42 |
| B.b点对应的溶液中大量存在:Na+、Ba2+、OH-、I- |
| C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HCO3- |
| D.d点对应的溶液中大量存在:Na+、K+、SO32-、Cl— |
B
解析试题分析:根据图像可知,a点溶于显中性,离子可以大量共存,A正确;b点溶于显酸性,则OH-不能大量共存,B不正确;c点溶于显中性,离子可以大量共存,C正确;d点溶于显碱性,离子可以大量共存,D正确,答案选B。
考点:考查离子共存的正误判断以及水的离子积常数的应用
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,难易适中,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑推理能力和应试能力。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
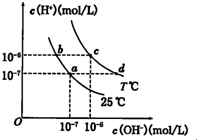 在不同温度下.水溶液中c(H+)与c(OH+)有如图所示的关系,下列说法中不正确的是( )
在不同温度下.水溶液中c(H+)与c(OH+)有如图所示的关系,下列说法中不正确的是( )| A、图中T>25 | B、b点溶液c(H+)一定比a点大 | C、c点对应的洛液中可能大量存在Al3+、Cl- | D、d点对应的溶液呈碱性 |
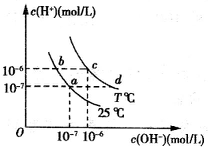 在不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示.下列有关说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示.下列有关说法中正确的是( )| A、若从a点到c点,可采用在水中加入酸的方法 | B、b点对应的醋酸中由水电离的c(H+)=10-6mol/L | C、c点对应溶液的Kw大于d点对应溶液的Kw | D、T℃时,0.05 mol?L-1的Ba(OH)2溶液的pH=11 |
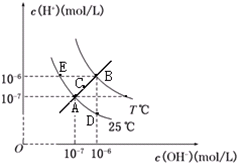 在不同温度下,水溶液中c(H+)与c(OH-)关系如图所示.下列说法不正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)关系如图所示.下列说法不正确的是( )| A、图中五点Kw间的关系:B>C>A=D=E | B、E点对应的水溶液中,可能有NH4+、Ba2+、Cl-、I-大量同时存在 | C、若处在B点时,将pH=2的硫酸溶液与pH=10的KOH溶液等体积混合,所得溶液呈中性 | D、若0.1 mol/L的NaHA溶液水溶液中c(H+)与c(OH-)关系如图D点所示,则溶液中有:c(HA-)>c(OH-)>c(A2-)>c(H2A) |
 在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是( )
在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是( ) 在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示.请回答下列问题:
在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示.请回答下列问题: