题目内容
19.氨的催化氧化是工业制硝酸的基础,其反应原理是4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.在该反应中,氧化剂是O2(填化学式),被氧化的物质是NH3(填化学式);若反应中消耗了2mol NH3,则生成2molNO.分析 4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O反应中N元素的化合价升高,O元素的化合价降低,结合氧化还原反应的有关概念分析.
解答 解:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O反应中N元素的化合价升高,被氧化,则NH3为还原剂,O元素的化合价降低,被还原,则氧气为氧化剂,由方程式可知,2 molNH3反应生成2molNO;
故答案为:O2;NH3;2.
点评 本题考查了氧化还原反应,侧重于基本概念的考查,注意根据化合价的变化分析,题目难度不大.

练习册系列答案
相关题目
10.北京奥运会“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述错误的是( )
| A. | 分子中的3个碳原子在一条直线上 | |
| B. | 在光照条件下能和氯气发生取代反应 | |
| C. | 分子中含有极性键和非极性键 | |
| D. | 丙烷和丁烷互为同系物 |
7.下列各组物质,不能用分液漏斗分离的是( )
| A. | 乙酸乙酯和水 | B. | 溴苯和水 | C. | 苯和甲苯 | D. | 硝基苯和水 |
14.结晶玫瑰是具有强烈玫瑰香气的香料,化学式为C10H9O2Cl3.它属于( )
| A. | 无机物 | B. | 有机物 | C. | 单质 | D. | 混合物 |
9.下列物质中,不能使酸性KMnO4溶液褪色的是( )
①乙烯 ②甲烷 ③乙苯 ④乙炔 ⑤苯酚 ⑥甲苯 ⑦苯 ⑧乙醇.
①乙烯 ②甲烷 ③乙苯 ④乙炔 ⑤苯酚 ⑥甲苯 ⑦苯 ⑧乙醇.
| A. | ②③④⑥ | B. | ②③④⑤⑥⑦⑧ | C. | ②④⑦ | D. | ②⑦ |
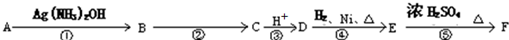
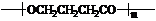 +nH2O.
+nH2O.
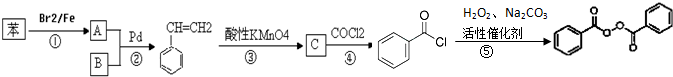
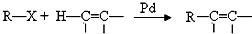
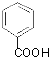 ;
;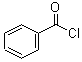 +H2O2$→_{碳酸钠}^{催化剂}$
+H2O2$→_{碳酸钠}^{催化剂}$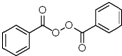 +2HCl;
+2HCl;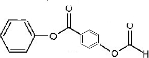 或
或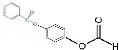 ;
; 的流程,无机物任选,注明反应条件.
的流程,无机物任选,注明反应条件.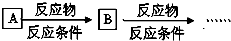
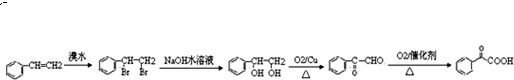 .
.