题目内容
8.(1)写出表示含有8个质子、10个中子的原子的化学符号8180.(2)元素周期表中,所含元素超过18种的周期是6、7.
分析 (1)质子数=原子序数,质子数+中子数=质量数,根据原子表示法来回答;
(2)第ⅢB族出现镧系和锕系元素,每格代表15中元素.
解答 解:(1)质子数=原子序数,质子数决定元素种类,所以含有8个质子的元素是O,并且质子数+中子数=质量数,所以该元素的质量数是18,表示为8180,故答案为:8180;
(2)元素周期表中,在第6、7(或六、七)周期的第ⅢB族出现镧系和锕系元素,所含元素种数最多,故答案为:6、7.
点评 本题考查原子的构成及元素在周期表中的位置和性质,注重基础,难度不大,明确元素周期表的结构是解答本题的关键.

练习册系列答案
相关题目
13.下列说法正确的是( )
| A. | 放热反应一定是断开反应物中的化学键吸收的能量比形成生成物中的化学键放出的能量少 | |
| B. | 1molH2SO4和1molBa(OH)2完全反应所放出的热量称为中和热 | |
| C. | 反应物的总能量低于生成物的总能量的化学反应为放热反应 | |
| D. | 在化学反应中需要加热的反应就是吸热反应 |

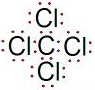 ,空间构型为正四面体.
,空间构型为正四面体.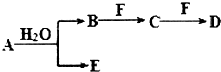 A、B、C、D、E、F为中学化学中的常见物质,且物质A由l~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题:(请用具体的元素符号及化学用语作答)
A、B、C、D、E、F为中学化学中的常见物质,且物质A由l~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题:(请用具体的元素符号及化学用语作答)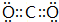 ;D的化学式为NaHCO3.
;D的化学式为NaHCO3. ,D属于共价化合物(填“共价”或“离子”);
,D属于共价化合物(填“共价”或“离子”);