题目内容
9.已知碳碳双键的碳原子上连有羟基的结构是不稳定的结构.A是一种直链一溴代物,F是五元环状内酯,其化学式为C4H6O2,有三种化学环境不同的氢(面积比1:1:1).物质间的转化关系如图所示.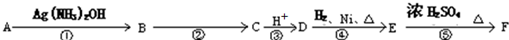
请根据上面的转化关系回答问题:
(1)化合物B的分子式是C4H5O2Br,化合物C的结构简式是HOCH2CH=CHCOONa.
(2)化合物A含有的官能团有溴原子、碳碳双键、醛基.
(3)②加入的试剂及反应条件是NaOH水溶液加热.
(4)写出 E在⑤反应中生成高分子化合物副反应的化学方程式nHOCH2CH2CH2COOH$→_{△}^{浓硫酸}$
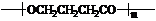 +nH2O.
+nH2O.(5)D有多种同分异构,满足下列条件的同分异构体有2种
①与碳酸氢钠溶液反应生成二氧化碳②与新制银氨溶液发生银镜反应.
分析 A能够与氢氧化二氨合银反应,说明A中含有醛基,A是一种直链一溴代物,最终生成的五元环状内酯的化学式为C4H6O2,且碳碳双键的碳原子上连有羟基的结构是不稳定的结构,可以推知A为BrCH2CH=CHCHO,F是五元环状内酯,其化学式为C4H6O2,有三种化学环境不同的氢(面积比1:1:1),可知F为 ,则E为HOCH2CH2CH2COOH,据反应条件推知D→E为碳碳双键与氢气的加成,D为HOCH2CH=CHCOOH,C酸化生成D,则B→C是在NaOH的水溶液中发生溴原子的水解,则C为HOCH2CH=CHCOONa,B为BrCH2CH=CHCOOH,据此分析.
,则E为HOCH2CH2CH2COOH,据反应条件推知D→E为碳碳双键与氢气的加成,D为HOCH2CH=CHCOOH,C酸化生成D,则B→C是在NaOH的水溶液中发生溴原子的水解,则C为HOCH2CH=CHCOONa,B为BrCH2CH=CHCOOH,据此分析.
解答 解:A能够与氢氧化二氨合银反应,说明A中含有醛基,A是一种直链一溴代物,最终生成的五元环状内酯的化学式为C4H6O2,且碳碳双键的碳原子上连有羟基的结构是不稳定的结构,可以推知A为BrCH2CH=CHCHO,F是五元环状内酯,其化学式为C4H6O2,有三种化学环境不同的氢(面积比1:1:1),可知F为 ,则E为HOCH2CH2CH2COOH,据反应条件推知D→E为碳碳双键与氢气的加成,D为HOCH2CH=CHCOOH,C酸化生成D,则B→C是在NaOH的水溶液中发生溴原子的水解,则C为HOCH2CH=CHCOONa,B为BrCH2CH=CHCOOH,
,则E为HOCH2CH2CH2COOH,据反应条件推知D→E为碳碳双键与氢气的加成,D为HOCH2CH=CHCOOH,C酸化生成D,则B→C是在NaOH的水溶液中发生溴原子的水解,则C为HOCH2CH=CHCOONa,B为BrCH2CH=CHCOOH,
(1)D为HOCH2CH=CHCOOH,C酸化生成D,则B→C是在NaOH的水溶液中发生溴原子的水解,则C为HOCH2CH=CHCOONa,B为BrCH2CH=CHCOOH,所以B的分子式为C4H5O2Br,故答案为:C4H5O2Br;HOCH2CH=CHCOONa;
(2)A为BrCH2CH=CHCHO,含有的官能团有溴原子、碳碳双键、醛基,故答案为:溴原子、碳碳双键、醛基;
(3)B→C是在NaOH的水溶液中加热发生溴原子的水解,故答案为:NaOH水溶液;加热;
(4)E为HOCH2CH2CH2COOH,能够通过酯化反应发生缩聚生成高分子化合物,反应方程式为n HOCH2CH2CH2COOH $→_{△}^{浓硫酸}$ 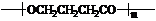 +n H2O,
+n H2O,
故答案为:n HOCH2CH2CH2COOH $→_{△}^{浓硫酸}$ 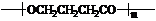 +n H2O;
+n H2O;
(5)D为HOCH2CH=CHCOOH,其同分异构体①与碳酸氢钠溶液反应生成二氧化碳,说明含有羧基,②与新制银氨溶液发生银镜反应,说明含有醛基,其可能的结构有OHCCH2CH2COOH和OHCCH(CH3)COOH两种,故答案为:2.
点评 本题考查有机物推断,综合分析确定F的结构是关键,再结合转化关系进行推断,侧重考查学生分析推理能力,需要学生熟练掌握官能团的性质与转化,难度中等.

 寒假学与练系列答案
寒假学与练系列答案 (1)T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示,根据图示可知:A与B反应生成C的化学方程式为A(g)+3B(g)?2C(g).
(1)T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示,根据图示可知:A与B反应生成C的化学方程式为A(g)+3B(g)?2C(g).(2)在80℃时,将0.40mol 的N2O4气体充入2L 已经抽空的固定容积的密闭容器中,发生如下反应:N2O4?2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
| A. | 反应中共消耗1.8 mol H2SO4 | B. | 气体甲中SO2与H2的体积比为4:1 | ||
| C. | 反应中共消耗97.5 g Zn | D. | 反应中共转移3 mol电子 |
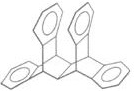 如图是一种形状酷似罗马两面神Janus的有机物结构简式如下,化学家建议将该分子叫做“Janusene”,有关Janusene的说法正确的是( )
如图是一种形状酷似罗马两面神Janus的有机物结构简式如下,化学家建议将该分子叫做“Janusene”,有关Janusene的说法正确的是( )| A. | Janusene的分子式为C30H24 | |
| B. | Janusene属于苯的同系物 | |
| C. | Janusene苯环上的一氯代物有6种 | |
| D. | Janusene既可使酸性高锰酸钾褪色,又可与H2发生加成反应 |
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
| A. | CH3Cl  | B. | CO2的电子式: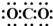 | ||
| C. | NH4Cl 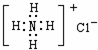 | D. | 氯原子的结构示意图: |
 W、X、Y、Z、M、G六种主族元素分属三个短周期,且原子序数依次增大.Y是地壳中含量最多的元素;M与Y同主族;G与Z形成的化合物是厨房常用的调味品;X的简单气态氢化物水溶液呈碱性.请回答下列问题:
W、X、Y、Z、M、G六种主族元素分属三个短周期,且原子序数依次增大.Y是地壳中含量最多的元素;M与Y同主族;G与Z形成的化合物是厨房常用的调味品;X的简单气态氢化物水溶液呈碱性.请回答下列问题: ,W、Y、Z、M、G形成的简单离子的半径大小顺序是S2->Cl->O2->Na+>H+(用相应的离子符号表示).
,W、Y、Z、M、G形成的简单离子的半径大小顺序是S2->Cl->O2->Na+>H+(用相应的离子符号表示).