题目内容
将NaCl、FeCl2、FeCl3、MgCl2、AlCl3、NH4Cl六种溶液,通过一步实验就能加以区别,并只用一种试剂,这种试剂是( )
| A、KSCN |
| B、BaCl2 |
| C、NaOH |
| D、HCl |
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:六种溶液含有的阳离子各不相同,但都是氯化物,因氯化钡与六种氯化物都不反应,利用金属氢氧化物的溶解性及颜色来鉴别,因又涉及到Al3+和Mg2+的鉴别,因此必需选强碱,以此来解答.
解答:
解:A.KSCN只能鉴别FeCl3,浅绿色溶液为FeCl2,其它不能鉴别,故A不选;
B.加入BaCl2溶液,与六种物质都不反应,不能鉴别,故B不选;
C.加入浓NaOH溶液,NaCl无现象,AlCl3先生成白色沉淀,沉淀然后溶解,FeCl2生成白色沉淀,然后迅速变成灰绿色,最后变成红褐色,FeCl3生成红褐色沉淀,MgCl2生成白色沉淀,NH4Cl有刺激性气体生成,现象各不相同,可鉴别,故C选;
D.均与盐酸不反应,现象相同,不能鉴别,故D不选;
故选C.
B.加入BaCl2溶液,与六种物质都不反应,不能鉴别,故B不选;
C.加入浓NaOH溶液,NaCl无现象,AlCl3先生成白色沉淀,沉淀然后溶解,FeCl2生成白色沉淀,然后迅速变成灰绿色,最后变成红褐色,FeCl3生成红褐色沉淀,MgCl2生成白色沉淀,NH4Cl有刺激性气体生成,现象各不相同,可鉴别,故C选;
D.均与盐酸不反应,现象相同,不能鉴别,故D不选;
故选C.
点评:本题考查物质的检验和鉴别,为高频考点,侧重于元素化合物知识的综合应用,为高考常见题型,注意把握相关物质的性质,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
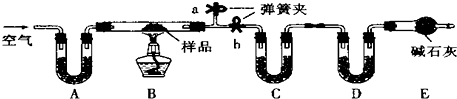
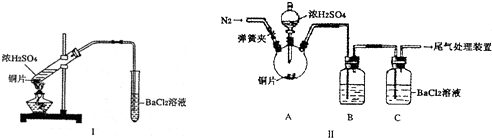
研究某一化学反应的实验装置如图:实验中产生的主要现象有:(1)D物质由黑色变成红色 (2)无水硫酸铜粉末放入无色透明的E中得到蓝色溶液 (3)F中的气体可用于工业合成氨.通过分析,A和B可能是( )

| A、浓硫酸和铜粒 |
| B、浓氨水和氧化钙 |
| C、浓盐酸和浓硫酸 |
| D、水和电石 |
下列离子方程式书写不正确的是( )
| A、常温下氯气与烧碱溶液反应:Cl2+2OH -═Cl-+ClO-+H2O |
| B、AlCl3溶液中加入足量的氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| C、铜与稀硝酸反应:Cu+2H+═Cu2++H2↑ |
| D、FeCl2溶液中加入氯水:2Fe2++Cl2═2Fe3++2Cl- |
不用任何试剂,只利用滴加顺序就能区分下列溶液的是( )
| A、硫酸和氢氧化钡 |
| B、碳酸钠和盐酸 |
| C、碳酸氢钠和盐酸 |
| D、氢氧化钠和盐酸 |
某气体由氢气、一氧化碳、甲烷中的一种或几种组成.点燃该气体后,在火焰上方罩一冷而干燥的烧杯,烧杯内壁出现水雾;把烧杯迅速倒转过来,注入少量澄清石灰水,振荡,石灰水变混浊.下列对气体组成的推断不正确的是( )
| A、可能三种气体都存在 |
| B、可能只有氢气 |
| C、可能是甲烷和一氧化碳的混合气体 |
| D、可能只有甲烷 |
下列有关生命的基础有机化学物质的说法中正确的是( )
| A、天然油脂在碱性条件下水解生成高级脂肪酸盐和甘油,故天然油脂是纯净物 |
| B、为检验淀粉是否发生水解,往其中加入氢氧化铜,未发现变红,说明淀粉没有发生水解 |
| C、氨基酸和蛋白质中都含有氨基和羧基,所以两者都具有两性 |
| D、鸡蛋白溶液在硫酸铵或硫酸铜的作用下都发生凝聚,两者在原理也完全相同 |