题目内容
6.下列关于电解质的说法中正确的是( )| A. | 纯水的导电性很差,所以水不是电解质 | |
| B. | SO2水溶液的导电性很好,所以SO2是电解质 | |
| C. | 熔融状态时铜的导电性很好,所以铜是电解质 | |
| D. | 硝酸钾在水中和熔融状态时都能导电,所以硝酸钾是电解质 |
分析 电解质是指:在水溶液中或熔融状态下能够导电的化合物.电解质水溶液中或熔融状态下能够导电,是因电解质自身可以离解成自由移动的离子;单质、混合物既不是电解质也不是非电解质.
解答 解:A.数存在微弱的电离,属于弱电解质,故A错误;
B.二氧化硫本身不能电离,其水溶液导电的原因是二氧化硫与水反应生成的亚硫酸导电,故二氧化硫是非电解质,故B错误;
C.铜是单质,既不是电解质也不是非电解质,故C错误;
D.硝酸钾是盐,是电解质,故D正确,
故选D.
点评 本题考查了电解质和非电解质的概念,以及电解质和金属导电的问题,属于易错题目,需要学习时认真归纳和总结,积累相关知识.

练习册系列答案
相关题目
10.如图实验与物质粒子大小无直接关系的是( )
| A. |  过滤 | B. |  渗析 | ||
| C. |  萃取 | D. |  丁达尔效应 |
17.一定温度下,在恒容容器中,对于反应2SO2(g)+O2(g)═2SO3(g),SO2和O2起始时分别为20mol和10mol,达到平衡时SO2的转化率为80%.若从SO3开始进行反应,在相同条件下,欲使平衡时各成分的质量分数与前平衡时相同,则起始时SO3的物质的量及SO3的转化率分别为( )
| A. | 10mol和10% | B. | 20mol和40% | C. | 20mol和20% | D. | 30mol和80% |
14.下列化学式表示的粒子对H2O的电离平衡不产生影响的是( )
| A. | 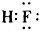 | B. | 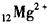 | C. |  | D. | OH- |
11.将20mL 0.3mol/L AgNO3溶液与10mL0.4mol/L CaC12 溶液混合,所得溶液中离子浓度关系正确的是( )
| A. | c(Ca2+)>c(Cl-)>c ( NO3-) | B. | c(Ca2+)>c ( NO3-)>c (Cl-) | ||
| C. | c(NO3-)>c ( Ca2+ )>c ( Cl-) | D. | c ( Cl-)>c(Ca2+)>c(NO3-) |
18.某物质的分子式为CxHyOz,取该物质ag在足量的O2中充分燃烧后,将产物全部通入过量的Na2O2中,若Na2O2固体的质量增加了bg,则下列说法正确的是( )
| A. | 若x>z则a>b | B. | x=y>z 则a<b | C. | x=z<y则a=b | D. | x<z=y则a<b |
15.硅是重要的半导体材料,构成了现代电子工业的基础.回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号M,该能层具有的原子轨道数为9、电子数为4.
(2)硅主要以硅酸盐、二氧化硅等化合物的形式存在于地壳中.
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以共价键相结合,其晶胞中共有8个原子,其中在面心位置贡献3个原子.
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备.工业上采用Mg2Si和NH4CI在液氨介质中反应制得SiH4,该反应的化学方程式为Mg2Si+4NH4Cl=SiH4+4NH3+2MgCl2
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是C-C键和C-H键较强,所形成的烷烃稳定.而硅烷中Si-Si键和Si-H键的键能较低,易断裂,导致长链硅烷难以生成.
②SiH4的稳定性小于CH4,更易生成氧化物,原因是C-H键的键能大于C-O键,C-H键比C-O键稳定.而Si-H键的键能却远小于Si-O键,所以Si-H键不稳定而倾向于形成稳定性更强的Si-O键.
(6)在硅酸盐中,SiO44-四面体(如下图a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式.图b为一种无限长单链结构的多硅酸根;其中Si原子的杂化形式为sp3.Si与O的原子数之比为1:3化学式为SiO32-.

(1)基态Si原子中,电子占据的最高能层符号M,该能层具有的原子轨道数为9、电子数为4.
(2)硅主要以硅酸盐、二氧化硅等化合物的形式存在于地壳中.
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以共价键相结合,其晶胞中共有8个原子,其中在面心位置贡献3个原子.
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备.工业上采用Mg2Si和NH4CI在液氨介质中反应制得SiH4,该反应的化学方程式为Mg2Si+4NH4Cl=SiH4+4NH3+2MgCl2
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 键能(KJ/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
②SiH4的稳定性小于CH4,更易生成氧化物,原因是C-H键的键能大于C-O键,C-H键比C-O键稳定.而Si-H键的键能却远小于Si-O键,所以Si-H键不稳定而倾向于形成稳定性更强的Si-O键.
(6)在硅酸盐中,SiO44-四面体(如下图a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式.图b为一种无限长单链结构的多硅酸根;其中Si原子的杂化形式为sp3.Si与O的原子数之比为1:3化学式为SiO32-.

16.下列分类正确的是( )
| A. |  | |||||||
| B. |  | |||||||
| C. |  | |||||||
| D. |
| |||||||
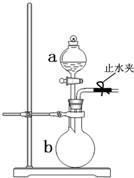 如图所示装置是实验室常用的气体制取装置.据图回答下列问题:
如图所示装置是实验室常用的气体制取装置.据图回答下列问题: