题目内容
在一定条件下,某化合物X受热分解:2X=A↑+2B↑+4C↑,测得反应后生成的混合气体对H2的相对密度为11.43.则在相同
条件下,X的相对分子质量是( )
条件下,X的相对分子质量是( )
分析:根据相对氢气的密度计算混合气体的平均摩尔质量,由方程式可知X与反应后的混合气体的物质的量之比为2:7,根据质量守恒可知X的质量等于反应后混合气体的质量,再根据M=
计算X的摩尔质量,据此解答.
| m |
| n |
解答:解:反应后生成的混合气体对H2的相对密度为11.43,
则混合气体的平均摩尔质量为2g/mol×11.43=22.86g/mol,
由方程式可知X与反应后的混合气体的物质的量之比为2:7,
根据质量守恒可知X的质量等于反应后混合气体的质量,故X的摩尔质量=
=80.01g/mol,
故X的相对分子质量为80.01,
故选C.
则混合气体的平均摩尔质量为2g/mol×11.43=22.86g/mol,
由方程式可知X与反应后的混合气体的物质的量之比为2:7,
根据质量守恒可知X的质量等于反应后混合气体的质量,故X的摩尔质量=
| 22.86g/mol×7mol |
| 2mol |
故X的相对分子质量为80.01,
故选C.
点评:本题考查相对分子质量的计算,难度不大,相对分子质量的计算方法多种多样,可以根据题目条件选择合适的计算方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
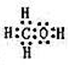
 H++HO2-
H++HO2-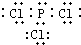


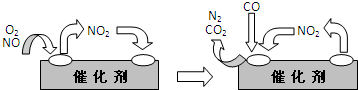
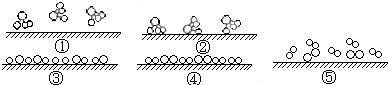
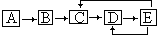
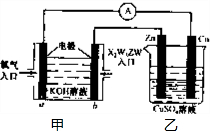 已知X、Y、Z、W四种短周期元素的原子半径依次减小.在周期表中X与Y、Y与Z均位同一周期的相邻位置;X的最外层电子数为次外层电子数的2倍;W分别能与X、Y、Z按一定原子数比形成电子总数为10的常见化合物.请判断X、Y、Z、W四种元素并回答下列问题:(要求用确定后的元素符号及有关化学用语表示)
已知X、Y、Z、W四种短周期元素的原子半径依次减小.在周期表中X与Y、Y与Z均位同一周期的相邻位置;X的最外层电子数为次外层电子数的2倍;W分别能与X、Y、Z按一定原子数比形成电子总数为10的常见化合物.请判断X、Y、Z、W四种元素并回答下列问题:(要求用确定后的元素符号及有关化学用语表示)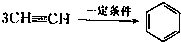 三聚氰胺也可以由氰胺(WXY分子中的W原子被氨基取代后可得氰胺)发生类似于乙炔的三聚反应而得到,三聚氰胺中无非极性键,含有量个氨基.请写出三聚氰胺结构简式:
三聚氰胺也可以由氰胺(WXY分子中的W原子被氨基取代后可得氰胺)发生类似于乙炔的三聚反应而得到,三聚氰胺中无非极性键,含有量个氨基.请写出三聚氰胺结构简式: