题目内容
近年来,科学家合成了一种稳定的氢铝化合物Al2H6。Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料。下列说法正确的是? (??? )

A、Al2H6可以燃烧,产物为氧化铝和水
B、1mol Al2H6中约含有4.8×1024个σ键
C、60g Al2H6中含铝原子约为1.2×1023个
D、Al2H6在固态时所形成的晶体是离子晶体
【答案】
A
【解析】
试题分析:A. 氢铝化合物Al2H6燃烧,其中Al变为Al2O3,H变为H2O。因此燃烧产物为氧化铝和水。正确。B、在Al2H6中Al化合价为+3价,H为-1价,每1mol Al2H6中含有6mol的Al—H键。即含3.6×1024个σ键.错误。C、Al2H6的式量为60,所以60g Al2H6的物质的量为1mol。含铝原子约为1.2×1024个.错误。D、根据Al2H6的熔点为150℃可确定在固态时所形成的晶体是分子晶体。离子晶体熔化要克服离子键,键能大,熔点高。错误。
考点:考查氢铝化合物Al2H6的结构与性质的关系的知识。

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
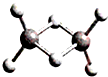 近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法肯定错误的是( )
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法肯定错误的是( )| A、Al2H6在固态时所形成的晶体是分子晶体 | B、Al2H6在空气中完全燃烧,产物为氧化铝和水 | C、氢铝化合物可能成为未来的储氢材料和火箭燃料 | D、氢铝化合物中可能存在组成为AlnH2n+2的物质(n为正整数) |
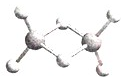 近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量.Al2H6球棍模型如图.下列说法肯定错误的是( )
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量.Al2H6球棍模型如图.下列说法肯定错误的是( )| A、Al2H6在固态时所形成的晶体是分子晶体 | B、氢铝化合物可能成为未来的储氢材料和火箭燃料 | C、Al2H6在空气中完全燃烧,产物为氧化铝和水 | D、Al2H6中含有离子键和极性共价键 |
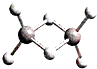 近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )
近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )| A、Al2H6可以燃烧,产物为氧化铝和水 | B、1mol Al2H6中约含有4.8×1024个σ键 | C、60g Al2H6中含铝原子约为1.2×1023个 | D、Al2H6在固态时所形成的晶体是离子晶体 |
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量。Al2H6球棍模型如下图。下列说法肯定错误的是( )
| A.Al2H6在固态时所形成的晶体是分子晶体 |
| B.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| C.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| D.Al2H6中含有离子键和极性共价键 |
