题目内容
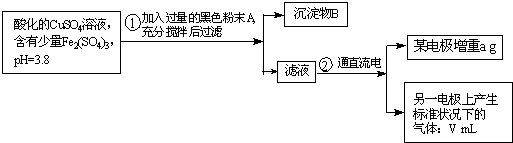
已知在pH为4~5的环境中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生欲用电解纯净CuSO4 溶液的方法来测定铜的相对原子质量。其实验过程如图所示:
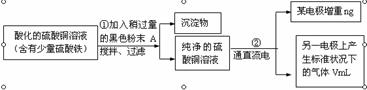
(1)步骤①所加的A的化学式为 ;加入A的作用是 _____________ ___ _ ___ ___。
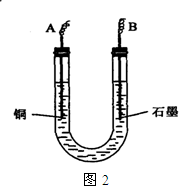
(2)步骤②中所用的部分仪器如图:则A应接在直流电源的 极(填“正”或“负” )。
(3)电解开始一段时间后,在U型管中观察到的现象有
;石墨电极上的电极反应式 。
(4)下列实验操作中必要的是(填字母) 。
A.称量电解前电极的质量
B.电解后,电极在烘干称重前,必须用蒸馏水冲洗
C.刮下电解后电极上析出的铜,并清洗、称重
D.电极在烘干称重的操作中必须按“烘干→称重→再烘干→再称重”进行
E.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为 (用带有n、V的计算式表示)。
(1)CuO;消耗H+,调节溶液的pH至4~5,使Fe(OH)3沉淀完全
(2)负
(3)溶液的蓝色变浅,A极变粗,B极上有气泡产生;4OH--4e-=2H2O+O2↑ (4)A、B、D、E
(5)11200n/V(3分)

练习册系列答案
相关题目
 已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用下图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体VmL.下列说法正确的是( )
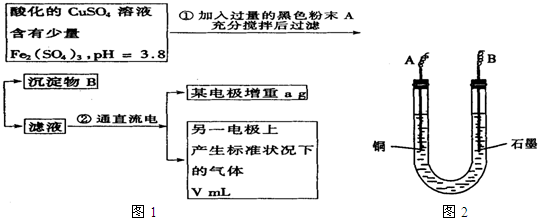
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用下图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体VmL.下列说法正确的是( ) 已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某同学拟用电解硫酸铜溶液的方法测定铜的相对原子质量.该同学向pH=3.8的含有硫酸铁杂质的硫酸铜溶液中加入过量的黑色粉末X,充分搅拌后将滤液用如图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL.下列说法正确的是( )
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某同学拟用电解硫酸铜溶液的方法测定铜的相对原子质量.该同学向pH=3.8的含有硫酸铁杂质的硫酸铜溶液中加入过量的黑色粉末X,充分搅拌后将滤液用如图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL.下列说法正确的是( )