��Ŀ����
8��ijѧϰС����������װ�ý���CO2�뱥��NaCO2��Һ��Ӧ�Ʊ�NaHCO3ʵ��
��1��ѡȡ��Ҫ��ʵ��װ�ã���ȷ������˳��Ϊ�ۢ٢ڣ�����ţ�
��2��Ϊȷ���ƵõĹ�����Ʒ�Ǵ�����NaHCO3��С��ͬѧ�������ʵ�鷽��
����������Ʒ��Һ�뱥�ͳ���ʯ��ˮ��Ӧ���۲�����
�ҷ���������Ʒ��Һ��BaCl4���۲�����
�����������pH��
�����������ط�����
��������������������������
��Ϊ�ж��ҷ����Ŀ����ԣ�ijͬѧ�÷�������NaHCO3���Ƶ���Һ����BaCl4��Һ�������Ͻ���ʵ�飬������£�
| NaHCO3��Һ BaCl3Ũ�� | 0.2mol•L-1 | 0.1mol•L-1 | 0.02mol•L-1 |
| 0.2mol•L-1 | ���� | ���� | �������� |
| 0.1mol•L-1 | ���� | �������� | ������ |
| 0.02mol•L-1 | �������� | ������ | ������ |
[��֪0.1mol•L-1NaHCO3��Һ�������c��CO32-��Ϊ0.0011mol•L-1��Ksp��BaCO3��=5.1��10-9]
�ڲ������ǵ����ӷ���ʽΪBa2++2HCO3-=BaCO3��+CO2��+H2O��
��ʹ��pH�ƽ��вⶨ�ı�������ȡ�������Ĺ�����Ʒ�ͷ�����NaHC03��Ʒ�ֱ��ܽ��ڵ�����ˮ�У��ֱ���pH�Ʋ�pH��
��3��ij��Һ�к���I-��Cl-�����ӣ�ȡһ������Ũ��Һ�������еμ�AgNO3��Һ����AgCl��ʼ����ʱ����Һ��$\frac{c��{I}^{-}��}{c��C{l}^{-}��}$Ϊ��4.8��10-7����֪Ksp��AgCl��=1.8��10-10��Ksp��Agl��=8.5��10-17��
���� ��1��������̼��Ʒ�Ӧ���ɶ�����̼������Ȼ��ƣ����������ӷ����ݴ�ѡ��������
��2���ٱ��ͳ���ʯ��ˮ��̼���ƺ�̼�����ƾ��ܷ�Ӧ����̼��Ƴ������ݴ˽��
�ڼ����ʱ��Һ�б�����Ũ����̼���Ũ�ȵij˻�����¶���̼�ᱵ���ܶȻ������Ƚϼ��ɣ�
�ڱ�������̼�����Ƶ������̼����������̼�ᱵ�������ٽ���̼������ĵ��룬ʹ��������̼����������ӵķ����ƶ����ݴ�д����Ӧ�����ӷ�Ӧ����ʽ��
�۱�����Ϊ�ⶨpH����̼����������ǿ�������Σ�������ȷ�Ƚϸߵ�pH�ƽ�����Ʒ��pHֵ��Ȼ�����������NaHC03��pHֵ���ɣ�
��3��AgCl��ʼ����ʱ��˵����Һ�е�c��I-����c��Cl-�����Ѵﵽ����״̬��������Һ��$\frac{c��{I}^{-}��}{c��C{l}^{-}��}$=$\frac{\frac{{K}_{sp}��AgI��}{c��A{g}^{+}��}}{\frac{{K}_{sp}��AgCl��}{c��A{g}^{+}��}}$=$\frac{{K}_{sp}��AgI��}{{K}_{sp}��AgCl��}$���ݴ˽��м��㣮
��� �⣺��1����Ϊ����װ�ã�������̼��Ʒ�Ӧ���ɶ�����̼������Ȼ��ƣ����������ӷ�����Ӧ��ѡȡ̼�����Ƴ�ȥ��������е�HCl������������˳��Ϊ���ۢ٢ڣ�
�ʴ�Ϊ���ۢ٢ڣ�
��2���ٱ��ͳ���ʯ��ˮ��̼���ƺ�̼�����ƾ��ܷ�Ӧ����̼��Ƴ������ʼ��������У�
�ʴ�Ϊ�������У�
��������Һ�������Ϻ���Һ�б�����Ũ��=$\frac{0.2mol/L}{2}$=0.1mol/L��0.1 mol•L-1 NaHC03��Һ�������c��CO32-��Ϊ0.0011 mol•L-1����Q=Q=c��Ba2+����c��CO32-��=$\frac{0.2}{2}$��0.0011=1.1��10-4��5.1��10-9���ʻ����������
�ʴ�Ϊ��Q=c��Ba2+����c��CO32-��=$\frac{0.2}{2}$��0.0011=1.1��10-4��5.1��10-9��
�ڱ�������̼�����Ƶ������̼����������̼�ᱵ�������Ӷ��ٽ���̼������ĵ��룬ʹ��������̼����������ӵķ����ƶ��������ӷ�Ӧ����ʽΪ��Ba2++2HCO3-=BaCO3��+CO2��+H2O��
�ʴ�Ϊ��Ba2++2HCO3-=BaCO3��+CO2��+H2O��
�۱�����Ϊ�ⶨpH��������̼����������ǿ�������Σ�������ȷ�Ƚϸߵ�pH�ƽ�����Ʒ��pHֵ��Ȼ�����������NaHC03��pHֵ�����Ƚϼ��ɣ�
�ʴ�Ϊ��ȡ�������Ĺ�����Ʒ�ͷ�����NaHC03��Ʒ�ֱ��ܽ��ڵ�����ˮ�У��ֱ���pH�Ʋ�pH��
��3��AgCl��ʼ����ʱ��˵����Һ�е�c��I-����c��Cl-�����Ѵﵽ����״̬����$\frac{c��{I}^{-}��}{c��C{l}^{-}��}$=$\frac{\frac{{K}_{sp}��AgI��}{c��A{g}^{+}��}}{\frac{{K}_{sp}��AgCl��}{c��A{g}^{+}��}}$=$\frac{{K}_{sp}��AgI��}{{K}_{sp}��AgCl��}$=$\frac{8.5��1{0}^{-17}}{1.8��1{0}^{-10}}$���ʴ�Ϊ��4.8��10-7��
���� ���⿼���������Ʊ���������������ۡ��������ܶȻ��ļ��㣬��Ŀ�Ѷ��еȣ���ȷ�Ʊ�ԭ�����������ܶȻ��ĸ�����㷽��Ϊ���ؼ�������֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ�����ѧ���ķ�����������������ѧʵ��������

| A�� | ���ˮ�еμӱ��͵��Ȼ�����Һ��ȡ���壺Fe3++3H2O�TFe��OH��3��+3H+ | |
| B�� | ̼����þ��Һ�м�������������������Һ��Mg2++2HCO3-+2OH-�TMgCO3��+CO32-+2H2O | |
| C�� | ��������Һ�м�������İ�ˮ��Al3++4NH3+2H2O�TAlO2-+4NH4+ | |
| D�� | ���۵⻯����ֽ�ڳ�ʪ�����б�����4I-+O2+2H2O�T2I2+4OH- |
��������⡿���á�˫�������ijɷ���ʲô��
���������롿���á�˫�������п�����Fe��Fe2O3��CaO��Ca��OH��2��CaCO3
��ʵ��̽��1��ȡ������Ʒ��ĥ���ô���������������մ�к�ɫ��ĩ��˵����˫��������һ����Fe�����ô����������������������ں���̽�����
��ʵ��̽��2��
| ʵ����� | ʵ������ | ʵ����� |
| ȡ����̽��ʵ��1�IJ�����������Թ��У���������ˮ | �Թ���ڲ����� | ������һ��û�� |

��ʵ����ۡ�����ڲ�����ɫ������˵�����õġ�˫�������к���Ca��OH��2���䷴Ӧ�Ļ�ѧ����ʽ��Na2CO3+Ca��OH��2=CaCO3��+2NaOH��
�����������ð������Һ��Ϊ��ɫ��˵�����õġ�˫�������к���Fe2O3��CaCO3��
| A�� | ˫��ˮ�м���ϡ�����KI��Һ��H2O2+2I-+2H+�TI2+2H2O | |
| B�� | ����Ȼ�þ��Һ��������ɫ���壺2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH- | |
| C�� | ���п��Ľ���Na¶���ڿ����У������ɹ����䰵��2Na+O2�TNa2O2 | |
| D�� | ��Ca��HCO3��2��Һ�м���������ռ���Һ�����ְ�ɫ������HCO3-+Ca2++OH-�TCaCO3��+H2O |
| A�� | �������ʶ��з�����������ԭ��Ӧ | |
| B�� | ���������ڷ�Ӧ��ת����2 mol���� | |
| C�� | �������ӵ�����Ǣ٣��ۣ��ܣ��� | |
| D�� | �������ӵ�����Ǣڣ��٣��ۣ��� |
| A�� | �����ʵ�����N2��CO������������ΪNA | |
| B�� | 1.7gH2O2�к��еĵ�����Ϊ0.9NA | |
| C�� | 10mL��������98%��H2SO4����ˮϡ����100mL��H2SO4����������Ϊ9.8% | |
| D�� | 1molCl2������������Ӧ��ת�Ƶĵ�����Ϊ3NA |
| A�� | S��P | B�� | Mg��Al | C�� | Na��Mg | D�� | Ne��He |
| A�� | ��������һ�������ɸ�CH2ԭ���ţ��ҷ���ͬһͨʽ���л���֮�以��Ϊͬϵ�� | |
| B�� | ���ۡ���ά�ء���Ȼ��֬�ȶ����ڻ���� | |
| C�� | ���ڱ����ӽṹ�������ԣ���˱����ܷ����ӳɷ�Ӧ | |
| D�� | �������������ԭ�Ӳ���һ��ƽ���ϣ���3��̼ԭ����һֱ���� |

 +R2C$\stackrel{����}{��}$
+R2C$\stackrel{����}{��}$ ��R�����
��RΪ�����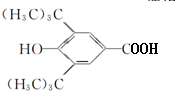 ��E�к��еĹ������������ǻ���ȩ����
��E�к��еĹ������������ǻ���ȩ���� $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$ +H2O���÷�Ӧ����Ϊ��ȥ��Ӧ��
+H2O���÷�Ӧ����Ϊ��ȥ��Ӧ�� +H2O���÷�Ӧ����Ϊ������Ӧ��
+H2O���÷�Ӧ����Ϊ������Ӧ��