题目内容
向某溶液中加BaCl2溶液,产生白色沉淀,加稀HNO3沉淀不消失,则溶液中( )
| A、一定含有SO42-或Ag+或其中一种 |
| B、可能含有SO42-或Ag+,不含SO32- |
| C、一定含有SO42-或SO32-或Ag+ |
| D、可能含有SO42-、SO32-、Ag+其中一种或两种 |
考点:常见阴离子的检验
专题:物质检验鉴别题
分析:BaCl2溶液中含有钡离子和氯离子,钡离子能形成硫酸钡、亚硫酸钡沉淀,氯离子能形成氯化银沉淀,三者加入稀HNO3后表示沉淀都不消失,据此进行判断溶液中可能含有的离子.
解答:
解:向某溶液中加入BaCl2溶液,产生白色沉淀,加稀HNO3沉淀不消失,白色沉淀可能是:BaSO4或BaSO3或AgCl;
白色沉淀若是硫酸钡,则原溶液中存在SO42-;
白色沉淀若是氯化银,则溶液中存在Ag+;
白色沉淀若是BaSO3,加入稀硝酸后BaSO3被氧化成硫酸钡,沉淀不会消失,所以原溶液中可能存在SO32-,
所以原溶液中可能含有SO42-、SO32-、Ag+其中一种或两种,所以D正确,
故选D.
白色沉淀若是硫酸钡,则原溶液中存在SO42-;
白色沉淀若是氯化银,则溶液中存在Ag+;
白色沉淀若是BaSO3,加入稀硝酸后BaSO3被氧化成硫酸钡,沉淀不会消失,所以原溶液中可能存在SO32-,
所以原溶液中可能含有SO42-、SO32-、Ag+其中一种或两种,所以D正确,
故选D.
点评:本题考查了常见阴阳离子的检验方法,题目难度不大,注意掌握常见离子的性质及正确的检验方法,明确检验离子存在时,必须排除干扰离子,确保检验方案的严密性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组液体混合物,用分液漏斗不能分开的是( )
| A、苯和水 | B、四氯化碳和水 |
| C、乙醇和水 | D、正己烷和水 |
下列物质中,属于同素异形体的是( )
| A、S2和S4 |
| B、CO和CO2 |
| C、16O和18O |
| D、H2和D2 |
下列化合物的电子式书写错误的是( )
A、氨气  |
B、四氯化碳  |
C、次氯酸 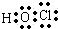 |
D、氯化钙  |
下列离子方程式正确的是( )
| A、Cl2与H2O反应:Cl2+H2O═2H++ClO-+Cl- |
| B、向Na2SiO3溶液中逐滴加入稀盐酸:2H++SiO32-═H2SiO3(胶体) |
| C、向AlCl3溶液中滴加氨水至过量:Al3++3OH-═Al(OH)3↓ |
| D、将铜片投入浓硝酸中:2NO3-+Cu+4H+═Cu2++2NO2↑+2H2O |
下列物质中属于共价化合物的是( )
| A、HNO3 |
| B、NaHSO4 |
| C、Na2O2 |
| D、I2 |
 如图,A是一种非金属单质,E是一种白色沉淀.据图填空:
如图,A是一种非金属单质,E是一种白色沉淀.据图填空: