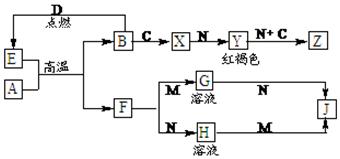
��Ŀ����
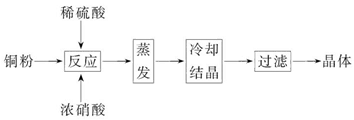
ij�����ĵ�������к���ͭ�����Ƚ��������Ϊʵ����Դ�Ļ������ò���Ч��ֹ������Ⱦ��������¹������̣�
��1����������H2O2��Ŀ���� ����pH�����м�����Լ������ ���ѧʽ����ʵ���ҽ��й��˲������õ��IJ��������� ��
��2�����CuSO4��Һ��ԭ���� ����CuSO4��Һ�м���һ������NaCl��Na2SO3���������ɰ�ɫ��CuCl������д���÷�Ӧ�Ļ�ѧ����ʽ ��
��3����ȡ���Ʊ���CuCl��Ʒ0.2500g����һ������0.5mol��L-1FeCl3��Һ�У�����Ʒ��ȫ�ܽ��ˮ20mL����0.1000mol��L-1��Ce��SO4��2��Һ�ζ��������յ�ʱ����Ce��SO4��2��Һ25.00mL���йصĻ�ѧ��ӦΪ��Fe3����CuCl��Fe2����Cu2����Cl����Ce4����Fe2����Fe3����Ce3���������CuCl��Ʒ���������� ��
��4��Fe3+����ˮ�ⷴӦFe3����3H2O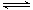 Fe(OH)3��3H�����÷�Ӧ��ƽ�ⳣ������ʽΪ ��
Fe(OH)3��3H�����÷�Ӧ��ƽ�ⳣ������ʽΪ ��
��1����Fe2+������Fe3�������ڵ���pHֵ��Cu2+���룻CuO��Cu(OH)2�ȣ�©�����ձ���������
��2��������Һ�е�H2O2������Ӱ����һ��CuCl������
2CuSO4��2NaCl��Na2SO3��H2O��2CuCl����2Na2SO4��H2SO4
��3��99.50% ��4��K��
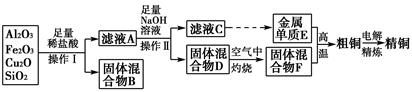
������������������ڵ�������к���ͭ�����Ƚ�����������Լ���ϡ��������Fe���������������Ӧ�������ܽ���ˮ�����ʣ���ȥ�����Ե����ʡ��ټ���H2O2������Fe2+����ΪFe3+.���ڵ�����Һ��pHֵ��ֽ��Cu2+���з��롣���ܽ�����Һ�����ԣ��ֲ������µ����ʣ�Ӧ�ü�������ʽ�������������Һ�е���ͬ���ɡ������CuO��Cu(OH)2��CuCO3��.��ʵ���ҽ��й��˲������õ��IJ���������©�����ձ�������������2������ϡ�����ܽ�����Һ�м�������ǿ�����Ե�H2O2���������ȥ����ʹ��ȡ��CuCl���������ʡ�����Ҫ��CuSO4��Һ���������H2O2����CuSO4��Һ�м���һ������NaCl��Na2SO3�����ɰ�ɫ��CuCl�����Ļ�ѧ����ʽΪ2CuSO4��2NaCl��Na2SO3��H2O��2CuCl����2Na2SO4��H2SO4����3���ɷ���ʽ�ɵù�ϵʽΪCuCl����Fe2������Ce4����n(Ce4��)="n(CuCl)=" c��V="0.1000mol/L" ��0.025L= 2.5��10-3mol.����m=n��M=2.5��10-3mol��99. 5=0.24875g.���Ը�CuCl��Ʒ����������Ϊ����0.24875�� 0.2500g����100%=99.50%����4����ѧƽ�ⳣ���ǿ��淴Ӧ�ﵽƽ��״̬ʱ��������Ũ����ָ���ij˻������Ӧ��Ũ�ȵ���ָ���˻��ıȡ���˸�ˮ�ⷴӦ��ƽ�ⳣ��K�� ��
��
���㣺���黯ѧʵ�������������ѧƽ�ⳣ���ı���ʽ�����ʵĴ��ȵļ��㼰��ҵ���̵�֪ʶ��

 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�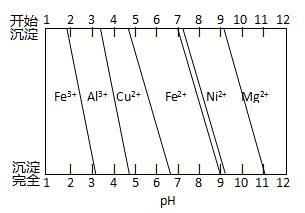
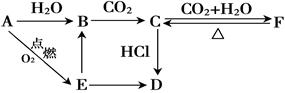
 C�� ��
C�� ��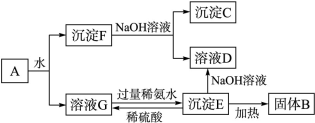
 Fe2O3+SO2��+SO3����
Fe2O3+SO2��+SO3����