题目内容
标准状况下的H2和CO的混合气体总体积4.48L,其总质量为4.3g.
求:(1)混合气体的平均摩尔质量
(2)混合气体所含质子的总物质的量
(3)若该混合气体与氧气恰好完全反应,则消耗标准状况下O2
求:(1)混合气体的平均摩尔质量
21.5
21.5
g/mol;(2)混合气体所含质子的总物质的量
2.2
2.2
mol,(3)若该混合气体与氧气恰好完全反应,则消耗标准状况下O2
2.24
2.24
L.分析:(1)根据
=
计算混合气体的平均摩尔质量;
(2)根据总物质的量结合原子构成计算质子的总物质的量;
(3)根据反应的方程式计算.
. |
| M |
| m总 |
| n总 |
(2)根据总物质的量结合原子构成计算质子的总物质的量;
(3)根据反应的方程式计算.
解答:解:(1)n(H2)+n(CO)=
=0.2mol,
m(H2)+m(CO)=4.3g,
混合气体的平均摩尔质量
=
=
=21.5g/mol,
故答案为:21.5;
(2)设H2的物质的量为x,CO的物质的量为y
则
解之得:x=0.05mol,y=0.15mol,
混合气体所含质子的总物质的量为:0.05mol×2+0.15mol×14=2.2mol,
故答案为:2.2;
(3)反应的方程式为:2H2+O2
2H2O,2CO+O2
CO2,
由方程式可知,消耗的O2的体积为混合气体体积的
,即V(O2)=
×4.48L=2.24L,
故答案为:2.24.
| 4.48L |
| 22.4L/mol |
m(H2)+m(CO)=4.3g,
混合气体的平均摩尔质量
. |
| M |
| m总 |
| n总 |
| 4.3g |
| 0.2mol |
故答案为:21.5;
(2)设H2的物质的量为x,CO的物质的量为y
则
|
解之得:x=0.05mol,y=0.15mol,
混合气体所含质子的总物质的量为:0.05mol×2+0.15mol×14=2.2mol,
故答案为:2.2;
(3)反应的方程式为:2H2+O2
| ||
| ||
由方程式可知,消耗的O2的体积为混合气体体积的
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:2.24.
点评:本题考查物质的量的相关计算,题目难度不大,注意平均摩尔质量的计算方法.

练习册系列答案
相关题目
 国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:
国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题: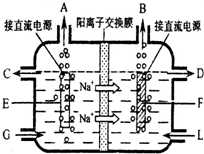 四川盛产井盐,由井盐提取的食盐是日常生活必需品,也是重要的化工原料.
四川盛产井盐,由井盐提取的食盐是日常生活必需品,也是重要的化工原料.