题目内容
5.铝镁加(Almagate)是一种制酸药,其组成为Al2Mg6(OH)14(CO3)2•4H2O,实验室可通过下列实验制备铝镁加.步骤1.称取63.5gMgSO4•7H2O(0.26mol),30.5gAl2(SO4)3•18H2O(0.046mol) 溶于400mL水中得到混合溶液A,另称取无水Na2CO352g溶于400mL水得到溶液B.
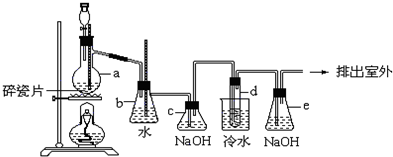
步骤2.将A、B两溶液同时等速滴加到盛有400mL90℃水的2L三颈烧瓶中,维持90℃,不断搅拌.
步骤3.抽滤,并用蒸馏水洗涤沉淀3~4次,100℃下干燥5h,得白色疏松固体24.3g.
(1)步骤2需缓慢滴加两种溶液并不断搅拌,其主要原因是使反应物充分接触,转化为指定产物.
(2)①步骤3抽滤时用到的硅酸盐质仪器有布氏漏斗、吸滤瓶.
②如何证明沉淀已洗涤干净取最后一次洗涤滤液滴入BaCl2溶液,若无白色沉淀说明已洗涤干净.
(3)本次实验所得产品产率为89.3%.
(4)铝镁加中和胃酸的离子方程式为Al2Mg6(OH)14(CO3)2•4H2O+18H+=2Al3++6Mg2++2CO2↑+20H2O.
分析 (1)从增大反应速率的影响因素分析,缓慢滴加两种溶液并不断搅拌是让物质充分接触加快反应速率;
(2)①抽滤装置包括吸滤瓶和布氏漏斗;
②检验沉淀已洗涤干净的实验操作是,取最后一次洗涤液,滴入氯化钡溶液,看是否生成白色沉淀分析判断是否洗涤干净;
(3)依据题干信息分析,依据镁离子、铝离子、碳酸根离子物质的量和铝镁加的组成为Al2Mg6(OH)14(CO3)2•4H2O,利用元素守恒分析判断参加反应离子的物质的量,依据全部反应的离子计算生成物的产率=$\frac{实际量}{理论量}$×100%;
(4)铝镁加中和胃酸反应生成二氧化碳、氯化镁、氯化铝和水.
解答 解:(1)将A、B两溶液同时等速滴加到盛有400mL90℃水的2L三颈烧瓶中,维持90℃,不断搅拌,使反应物充分接触,转化为指定产物,
故答案为:使反应物充分接触,转化为指定产物;
(2)①步骤3.抽滤,并用蒸馏水洗涤沉淀3~4次,用到的硅酸盐质仪器是玻璃仪器,主要有布氏漏斗、吸滤瓶,
故答案为:布氏漏斗;吸滤瓶;
②抽滤,并用蒸馏水洗涤沉淀3~4次,证明沉淀已洗涤干净的实验设计为:取最后一次洗涤滤液滴入BaCl2溶液,若无白色沉淀说明已洗涤干净,
故答案为:取最后一次洗涤滤液滴入BaCl2溶液,若无白色沉淀说明已洗涤干净;
(3)称取63.5gMgSO4•7H2O(0.26mol),30.5gAl2(SO4)3•18H2O(0.046mol) 溶于400mL水中得到混合溶液A,另称取无水Na2CO352g溶于400mL水得到溶液B,n(Mg)0.26mol,n(Al)=0.046mol×2=0.092mol,n(CO32-)=$\frac{52g}{106g/mol}$=0.49mol,分析化学式可知,镁元素全部转化到铝镁加,依据镁元素物质的量计算铝镁加的理论量=0.26mol×$\frac{1}{6}$×628g/mol=27.2g,
生成物的产率=$\frac{实际量}{理论量}$×100%=$\frac{24.3g}{27.2g}$×100%=89.3%;
故答案为:89.3%;
(4)铝镁加中和胃酸反应生成二氧化碳、氯化镁、氯化铝和水,反应的化学方程式为:Al2Mg6(OH)14(CO3)2•4H2O+18H+=2Al3++6Mg2++2CO2↑+20H2O,
故答案为:Al2Mg6(OH)14(CO3)2•4H2O+18H+=2Al3++6Mg2++2CO2↑+20H2O.
点评 本题考查了物质制备的实验过程分析判断,化学式的确定,主要是制备步骤和反应产物的理解应用,掌握基础是解题关键,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | SO32-→S | B. | HCl→Cl2 | C. | Fe→Fe3+ | D. | NO→NO2 |
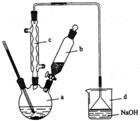 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)在a中加入15mL无水苯和少量铁屑.在b中小心加入4.0mL 液溴.向a中滴入几滴液溴,有白雾产生,是因为生成了HBr气体.继续滴加至液溴滴完.装置d中NaOH溶液的作用是吸收HBr和Br2.
(2)反应过程中,a外壁温度升高,为提高原料利用率,利用温度计控制温度,适宜的温度范围为(填序号)C.
A.>156℃B. 59℃-80℃C.<59℃
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是除去未反应的Br2;
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是干燥或除去粗溴苯中的水.
(4)经过上述分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,下列操作中必须的是C(填入正确选项前的字母).
A.重结晶 B.过滤 C.蒸馏 D.萃取.

 对叔丁基苯酚
对叔丁基苯酚 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚.实验步骤如下:反应物和产物的相关数据列表如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚.实验步骤如下:反应物和产物的相关数据列表如下: .该反应过于激烈,放出大量热,常使实验的产率降低,可能的原因是由于叔丁基氯挥发导致产率降低.
.该反应过于激烈,放出大量热,常使实验的产率降低,可能的原因是由于叔丁基氯挥发导致产率降低.