题目内容
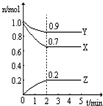
 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:(1)该反应的化学方程式为
3 X+Y  2 Z
2 Z
 2 Z
2 Z3 X+Y  2 Z
2 Z
. 2 Z
2 Z(2)反应开始至2min,气体Z的平均反应速率为
0.05 mol?(L?min)-1
0.05 mol?(L?min)-1
.分析:(1)根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式;
(2)根据v=
计算反应速率.
(2)根据v=
| △c |
| △t |
解答:解:(1)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,
且△n(X):△n(Y):△n(Z)=0.3mol:0.1mol:0.2mol=3:1:2,则反应的化学方程式为:3X+Y 2Z,
2Z,
故答案为:3X+Y 2Z;
2Z;
(2)v(Z)=
=0.05mol?(L?min)-1,故答案为:0.05mol?(L?min)-1.
且△n(X):△n(Y):△n(Z)=0.3mol:0.1mol:0.2mol=3:1:2,则反应的化学方程式为:3X+Y
 2Z,
2Z,故答案为:3X+Y
 2Z;
2Z;(2)v(Z)=
| ||
| 2min |
点评:本题考查化学平衡图象分析题目,题目难度不大,注意分析各物质的量的变化曲线,把握化学方程式的判断方法.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
 2Z
2Z 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白: 2Z
2Z 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空: 2Z
2Z 某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示.下列说法在不正确的是( )
某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示.下列说法在不正确的是( )