题目内容
锗(Ge)、锡(Sn)、铅(Pb)与碳、硅两元素同位于第ⅣA族,其原子序数按锗、锡、铅的顺序依次增大,则下列推断一定不正确的是
A.锗、锡在空气中不反应,铅在空气中表面生成一层氧化铅
B.锗与盐酸不反应,锡、铅能与盐酸反应
C.锗、锡、铅的+4价氢氧化物的碱性:Ge(OH)4<Sn(OH)4<Pb(OH)4
D.锗、锡、铅的金属性依次减弱
D
【解析】
试题分析:A.若锗、锡在空气中不反应,而铅活动性比锗、锡强,所以铅在空气中表面生成一层氧化铅,正确;B.锗与盐酸不反应,而锡、铅活动性比锗强,所以可能都能与盐酸反应,正确;C.从上到下,元素的金属性逐渐增强,所以锗、锡、铅的+4价氢氧化物的碱性:Ge(OH)4<Sn(OH)4<Pb(OH)4,正确;D.由于从上到下元素原子的核外电子层数逐渐增多,所以元素的金属性逐渐增强,故锗、锡、铅的金属性依次增强,错误。
考点:考查同族元素的单质及化合物的性质比较的知识。

练习册系列答案
相关题目
下列根据实验操作和现象所得出的结论错误的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里 出现凝胶 | 酸性:盐酸>硅酸 |
B | 向蛋白质溶液中滴加饱和CuSO4溶液 | 有固体析出 | 蛋白质发生变性 |
C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁不与浓硫酸反应 |
D | 向某溶液中先滴加KSCN溶液,再滴加少量氯水 | 先无明显现象, 后溶液变成血红色 | 溶液中含有Fe2+,没有Fe3+ |
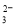
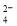
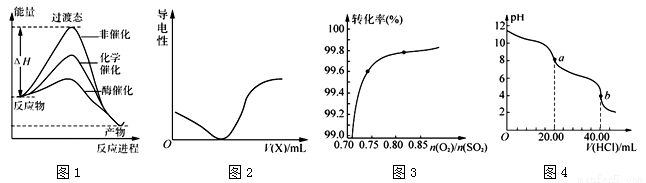 A.由图1所示曲线可知,化学催化比酶催化的效果好
A.由图1所示曲线可知,化学催化比酶催化的效果好 2SO3(g)转化关系(图3)中,纵坐标表示O2的转化率
2SO3(g)转化关系(图3)中,纵坐标表示O2的转化率