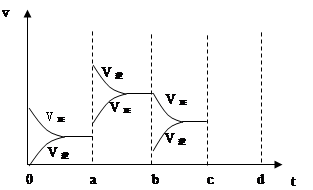��Ŀ����
��16�֣� ��1����2mol SO2��1mol O2����2L�ܱ������з������·�Ӧ��
2SO2+O2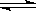 2SO3��H��0
2SO3��H��0
���ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯���������ͼ��ʾ��
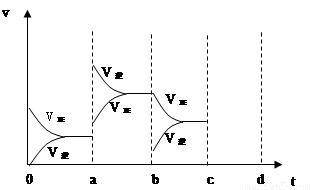
��1��a b�����иı������������ ���� ��
��2��b c�����иı������������ ��
��3��������ѹǿʱ����Ӧ�ٶȱ仯�������c~d����
(4) �ﵽ��һ��ƽ��ʱ�����ƽ��ʱSO3��Ũ��Ϊ0.5mol/L�������������µ�ƽ�ⳣ����SO2��ת���ʡ���Ҫ��д��������̣�
(��16�֣�
��1�����£���(2)��С SO3Ũ�ȣ���
(3) ��ͼ����2�֣���
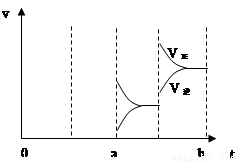
(4) 4�� 50% ����10�֣�
��������
�����������2mol SO2��1mol O2����2L�ܱ������з������·�Ӧ��
2SO2+O2 2SO3��H��0
2SO3��H��0
a��b�ı仯�����Կ��������淴Ӧ���ʶ�������ͻԾ�����ң��淴Ӧ���ʴ�������Ӧ���ʣ����ڸ÷�Ӧ���ȣ�����ab�������ı������£�b��c�ı仯���淴Ӧ����ͻԾ�½�������Ӧ�����������ͣ��ı�����������Ǽ�С SO3Ũ�ȣ�
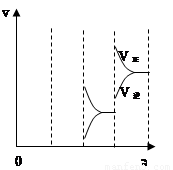
������ѹǿʱ����Ӧ�ٶȱ仯�������ͼ:
�ﵽ��һ��ƽ��ʱ�����ƽ��ʱSO3��Ũ��Ϊ0.5mol/L��
2SO2 +
O2  2SO3��H��0
2SO3��H��0
��ʼŨ�� 1 0.5 0
�仯Ũ�� 0.5 0.25 0.5
ƽ��Ũ�� 0.5 0.25 0.5
�������µ�ƽ�ⳣ��K=C2(SO3)/C2(SO2)*C(O2) =4��
SO2��ת����=0.5/1=50%��
���㣺��ѧƽ�ⳣ�� ��Ӧ���ʵ�Ӱ������
��������ѧƽ�ⳣ������ָ��һ���¶��£����淴Ӧ���۴�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ��Ҳ���ܷ�Ӧ����ʼŨ�ȴ�С����ﵽƽ�⣬��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ�Ǹ���������K��ʾ����������л�ѧƽ�ⳣ����ƽ�ⳣ��һ����Ũ��ƽ�ⳣ����ѹǿƽ�ⳣ����
����дƽ�ⳣ������ʽʱ��Ҫע���������⣺
�� ��Ӧ��ƽ�ⳣ������ʽʱ��ϡ��Һ�е�ˮ����Ũ�ȿɲ�д����Ϊϡ��Һ���ܶȽӽ���1 g/mL��ˮ�����ʵ���Ũ��Ϊ55.6 mol/L���ڻ�ѧ�仯�����У�ˮ���ĸı��ˮ��Ũ�ȱ仯Ӱ�켫С������ˮ��Ũ����һ���������˳����ɹ鲢��ƽ�ⳣ����ȥ��
���ڷ�ˮ��Һ�еķ�Ӧ���ܼ���Ũ��ͬ���dz�����
�� ����Ӧ���й������ʲμ�ʱ�����Ӽ����ײֻ���ڹ��������У���������ʵ���Ũ�ȶԷ�Ӧ���ʺ�ƽ��û��Ӱ�죬��ˣ�����ġ�Ũ�ȡ���Ϊ��������ƽ�ⳣ������ʽ�У��Ͳ�д�����Ũ�ȡ�
�� ��ѧƽ�ⳣ������ʽ�뻯ѧ����ʽ����д��ʽ�йء�ͬһ����ѧ��Ӧ��������д�ķ�ʽ��ͬ������Ӧ�������Ļ�ѧ��������ͬ��ƽ�ⳣ���Ͳ�ͬ��������Щƽ�ⳣ����������㡣
�� ��ͬ�Ļ�ѧƽ����ϵ����ƽ�ⳣ����һ����ƽ�ⳣ����˵���������ƽ��Ũ�Ƚϴ�Ӧ���ƽ��Ũ����Խ�С����������Ӧ���еý���ȫ����ˣ�ƽ�ⳣ���Ĵ�С���Ա�ʾ��Ӧ���еij̶ȡ�
��һ����ΪK>10^5��Ӧ����ȫ���������淴Ӧ����K<10^(-5)��Ӧ���ѽ��У�������Ӧ����
ƽ�ⳣ������ֵ��С�����жϷ�Ӧ���еij̶ȡ�

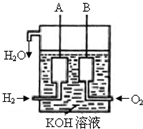 ��֪��25��C��1.013��105Pa�£�1mol������ȫȼ������Һ̬ˮ�ų�285kJ����������ش��������⣺
��֪��25��C��1.013��105Pa�£�1mol������ȫȼ������Һ̬ˮ�ų�285kJ����������ش��������⣺ 2SO3��H��0
2SO3��H��0