��Ŀ����
�������ƣ�NaClO2����һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڣ�ijͬѧ�������Ϻ��������NaClO2����Ҫ�������£�

��1��˫��ˮ�ĵ���ʽΪ �����з�����Ӧ�Ļ�ԭ���� ���ѧʽ����
��2�����з�Ӧ�����ӷ���ʽ�� ��
��3��ClO2��һ�ָ�Чˮ�������������������ƺ�ϡ����Ϊԭ���Ʊ���
��д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
���о�����������Ӧ��ʼʱ����Ũ��Խ�������������Cl2�ĺ���Խ������������ԭ��Ӧ���ɷ�������ԭ���� ��
��4��NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ����������ǰ���NaClO2�����������Һ���ֱ�������FeSO4��Һ��Ӧʱ������Fe2+�����ʵ��� �����ͬ����������ͬ�������жϡ���

��1��˫��ˮ�ĵ���ʽΪ
��2�����з�Ӧ�����ӷ���ʽ��
��3��ClO2��һ�ָ�Чˮ�������������������ƺ�ϡ����Ϊԭ���Ʊ���
��д���÷�Ӧ�Ļ�ѧ����ʽ��
���о�����������Ӧ��ʼʱ����Ũ��Խ�������������Cl2�ĺ���Խ������������ԭ��Ӧ���ɷ�������ԭ����
��4��NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ����������ǰ���NaClO2�����������Һ���ֱ�������FeSO4��Һ��Ӧʱ������Fe2+�����ʵ���
���㣺���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ��,�Ʊ�ʵ�鷽�������
ר�⣺ʵ�������
������������ͼ��֪��Ӧ��Ӧ��ΪNaClO3��Na2SO3������A��Һ������C1O2��Na2SO4��Һ����Ӧ���ӷ���ʽΪ2H++SO32-+2ClO3-=2C1O2+SO42-+H2O���������Ӹ�Ĥ���أ��ӷ�Ӧ��֪�õ���������ɡ��Ӣ�֪�м����ɣ��������������ɣ����Ԣ�Ϊ��������Ʊ����ǵ��ˮ��AΪ���ᣬaΪ������bΪ������C1O2����������ڼ��������·�Ӧ����NaClO2��������
��1��˫��ˮΪ���ۻ���������д��������������һ��O-O���������������Ʊ��������������ƣ�
��2������ClO2��NaClO2�Ļ��ϼۼ�����aΪ����������д�����ӷ���ʽ��
��3�����������ƺ�ϡ���ᷴӦ����ClO2��NaCl��ˮ��
�ڸ��������Ϣ���о�����������Ӧ��ʼʱ����Ũ��Խ�������������Cl2�ĺ���Խ��Ϣٷ���ʽ���з������
��4���ѱ��ʺ�δ���ʵ�NaClO2��Fe2+��Ӧ������Cl-������ת�Ƶ����غ��жϣ�
��1��˫��ˮΪ���ۻ���������д��������������һ��O-O���������������Ʊ��������������ƣ�
��2������ClO2��NaClO2�Ļ��ϼۼ�����aΪ����������д�����ӷ���ʽ��
��3�����������ƺ�ϡ���ᷴӦ����ClO2��NaCl��ˮ��
�ڸ��������Ϣ���о�����������Ӧ��ʼʱ����Ũ��Խ�������������Cl2�ĺ���Խ��Ϣٷ���ʽ���з������
��4���ѱ��ʺ�δ���ʵ�NaClO2��Fe2+��Ӧ������Cl-������ת�Ƶ����غ��жϣ�
���
�⣺������ͼ��֪��Ӧ��Ӧ��ΪNaClO3��Na2SO3������A��Һ������C1O2��Na2SO4��Һ����Ӧ���ӷ���ʽΪ2H++SO32-+2ClO3-=2C1O2+SO42-+H2O���������Ӹ�Ĥ���أ��ӷ�Ӧ��֪�õ���������ɡ��Ӣ�֪�м����ɣ��������������ɣ����Ԣ�Ϊ��������Ʊ����ǵ��ˮ��AΪ���ᣬaΪ������bΪ������C1O2����������ڼ��������·�Ӧ����NaClO2��������
��1��˫��ˮ�ǹ��ۻ���������ʽΪ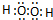 ��������ͼ��֪��Ӧ��Ӧ��ΪNaClO3��Na2SO3������A��Һ������C1O2��Na2SO4��Һ����Ӧ���ӷ���ʽΪ2H++SO32-+2ClO3-=2C1O2+SO42-+H2O������Na2SO3���л�ԭ���ǻ�ԭ������ClO3-��ԭΪC1O2��
��������ͼ��֪��Ӧ��Ӧ��ΪNaClO3��Na2SO3������A��Һ������C1O2��Na2SO4��Һ����Ӧ���ӷ���ʽΪ2H++SO32-+2ClO3-=2C1O2+SO42-+H2O������Na2SO3���л�ԭ���ǻ�ԭ������ClO3-��ԭΪC1O2��
�ʴ�Ϊ��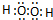 ��Na2SO3��
��Na2SO3��
��2�������з�Ӧ����������Ϣ��֪������NaClO2������һ����ClO2��NaClO2�����ϼ۽��ͣ�����ԭ����H2O2�ض�����������������������Ӧ��ClO2����������������ԭ��Ӧ��H2O2�ǻ�ԭ��������������Ӧ�����ݵ���ת���غ��֪4n��ClO2��=n��HCl�������Է�Ӧ����ʽΪ��2NaOH+2ClO2+H2O2=2 NaClO2+2H2O+O2�������ӷ���ʽ��2ClO2+H2O2+2OH-=2ClO2-+O2��+2H2O��
�ʴ�Ϊ��2ClO2+H2O2+2OH-=2ClO2-+O2��+2H2O��
��3�����������ƺ�ϡ���ᷴӦ����ClO2��NaCl��ˮ����ѧ����ʽΪ5NaClO2+4HCl=5NaCl+4ClO2��+2H2O���ʴ�Ϊ��5NaClO2+4HCl=5NaCl+4ClO2��+2H2O��
��5NaClO2+4HCl=5NaCl+4ClO2��+2H2O��Ӧ�У�ClO2-���������ԣ�ClO2-������������Һ�����Ժ�Ũ�ȵ��������ǿ�����Cl-�������õ�Cl2�����ӷ���ʽΪClO2-+3Cl-+4H+=2Cl2+2H2O�������о�����������Ӧ��ʼʱ����Ũ��Խ�������������Cl2�ĺ���Խ��
�ʴ�Ϊ��ClO2-�������Ի�Cl-�Ļ�ԭ������Һ�����Ժ�Ũ�ȵ��������ǿ�����Cl-�������õ�Cl2��
��4��Fe2+�����ǰ���NaClO2��Ӧ�����Ļ�ԭ���ﶼ��NaCl�����ݵ����غ����ĵ�Fe2+���ʵ���Ӧ��ͬ���ʴ�Ϊ����ͬ��
��1��˫��ˮ�ǹ��ۻ���������ʽΪ
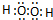 ��������ͼ��֪��Ӧ��Ӧ��ΪNaClO3��Na2SO3������A��Һ������C1O2��Na2SO4��Һ����Ӧ���ӷ���ʽΪ2H++SO32-+2ClO3-=2C1O2+SO42-+H2O������Na2SO3���л�ԭ���ǻ�ԭ������ClO3-��ԭΪC1O2��
��������ͼ��֪��Ӧ��Ӧ��ΪNaClO3��Na2SO3������A��Һ������C1O2��Na2SO4��Һ����Ӧ���ӷ���ʽΪ2H++SO32-+2ClO3-=2C1O2+SO42-+H2O������Na2SO3���л�ԭ���ǻ�ԭ������ClO3-��ԭΪC1O2���ʴ�Ϊ��
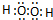 ��Na2SO3��
��Na2SO3����2�������з�Ӧ����������Ϣ��֪������NaClO2������һ����ClO2��NaClO2�����ϼ۽��ͣ�����ԭ����H2O2�ض�����������������������Ӧ��ClO2����������������ԭ��Ӧ��H2O2�ǻ�ԭ��������������Ӧ�����ݵ���ת���غ��֪4n��ClO2��=n��HCl�������Է�Ӧ����ʽΪ��2NaOH+2ClO2+H2O2=2 NaClO2+2H2O+O2�������ӷ���ʽ��2ClO2+H2O2+2OH-=2ClO2-+O2��+2H2O��
�ʴ�Ϊ��2ClO2+H2O2+2OH-=2ClO2-+O2��+2H2O��
��3�����������ƺ�ϡ���ᷴӦ����ClO2��NaCl��ˮ����ѧ����ʽΪ5NaClO2+4HCl=5NaCl+4ClO2��+2H2O���ʴ�Ϊ��5NaClO2+4HCl=5NaCl+4ClO2��+2H2O��
��5NaClO2+4HCl=5NaCl+4ClO2��+2H2O��Ӧ�У�ClO2-���������ԣ�ClO2-������������Һ�����Ժ�Ũ�ȵ��������ǿ�����Cl-�������õ�Cl2�����ӷ���ʽΪClO2-+3Cl-+4H+=2Cl2+2H2O�������о�����������Ӧ��ʼʱ����Ũ��Խ�������������Cl2�ĺ���Խ��
�ʴ�Ϊ��ClO2-�������Ի�Cl-�Ļ�ԭ������Һ�����Ժ�Ũ�ȵ��������ǿ�����Cl-�������õ�Cl2��
��4��Fe2+�����ǰ���NaClO2��Ӧ�����Ļ�ԭ���ﶼ��NaCl�����ݵ����غ����ĵ�Fe2+���ʵ���Ӧ��ͬ���ʴ�Ϊ����ͬ��
���������⿼������NaClO2���Ʊ�ʵ��Ĺ�ҵ��ƣ�Ϊ�߿��������ͣ�������ѧ���ķ���������ʵ�������ͼ��������Ŀ��飬�������ʵ�������������������ԭ��ӦΪ������Ĺؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 �»ƸԱ����ܾ�ϵ�д�
�»ƸԱ����ܾ�ϵ�д�
�����Ŀ
���л�ѧ������д��ȷ���ǣ�������
A�������ӵĽṹʾ��ͼ�� | ||
B����Ϊ���ԭ�������ⶨ����̼���أ�
| ||
C���Ȼ�þ�ĵ���ʽ�� | ||
D���õ���ʽ��ʾ�Ȼ�����ӵ��γɹ��̣� + + �� ��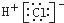 |
��һ�������£���0.1mol A2��0.3mol B2���뵽һ����������10L�ܱ������У��������·�Ӧ��A2��g��+3B2��g��?2AB3��g������ͬ�¶��´ﵽƽ��ʱAB3�����������ͼ�������й��ƶ���ȷ���ǣ�������


| A��ƽ�ⳣ����K��T1����K��T2�� |
| B����Ӧ�ʱ䣺��H��0 |
| C������Ӧ���ʣ�v��T1����v��T2�� |
| D��T1ʱƽ��Ũ�ȣ�c��AB3��=0.08 mol?L-1 |
���������У����ڹ��ۻ�������ǣ�������
| A��Cl2 |
| B��NH4Cl |
| C��H2SO4 |
| D��KOH |
ij�ֻ��������ܺ���N2��HCl��CO����ͨ������NaHCO3��Һ������CuO����������û�б仯��Ȼ��ͨ������Na2O2���壬���������С�����ͨ�����ȵ�Cu����ַ�Ӧ����������ּ��٣�������ʣ�����壬���¶Ի����������ж���ȷ���ǣ�������
| A��һ��û��N2��CO��HCl������1�� |
| B��һ����N2��HCl��CO |
| C��һ����N2��CO��HCl������1�� |
| D��һ����N2��CO��û��HCl |



 Ŀǰ������ʹ�õĵ��Ʒ�ֲ��٣�����Ǧ���ص�ʹ�������
Ŀǰ������ʹ�õĵ��Ʒ�ֲ��٣�����Ǧ���ص�ʹ�������