题目内容
2.下列各溶液中,Na+浓度最大的是( )| A. | 8 L 0.2mol/L的Na2SO4溶液 | B. | 8 L0.15mol/L的Na3PO4溶液 | ||
| C. | 10 L0.1 mol/L的Na2CO3溶液 | D. | 2 L 0.5mol/L的NaCl溶液 |
分析 结合物质的构成及溶质的浓度计算离子的浓度,以此来解答.
解答 解:A.Na+浓度为0.2mol/L×2=0.4mol/L;
B.Na+浓度为0.15mol/L×3=0.45mol/L;
C.Na+浓度为0.1mol/L×2=0.2mol/L;
D.Na+浓度为0.5mol/L×1=0.5mol/L,
显然D中最大,
故选D.
点评 本题考查物质的浓度的计算,为高频考点,把握物质的构成及离子浓度的计算为解答的关键,侧重分析与计算能力的考查,注意离子浓度与溶液体积无关,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
12.“材料“的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义.请回答下列问题:
Ⅰ.(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成为CaO•3MgO•4SiO2.
(2)高分子材料可以分成无机高分子材料和有机高分子材料.[AlFe(OH)nCl6-n]m属于无机高分子材料,是一种新型高效净水剂,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为+3.
Ⅱ.高纯二氧化硅可用来制造光纤.某稻壳灰的成分如下表:
通过如下流程可由稻壳灰制备较纯净的二氧化硅: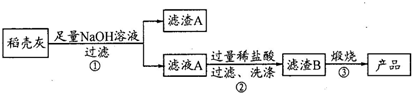
请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物的种类最多有3类,其中SiO2为酸性氧化物(填氧化物的类别)
(2)滤渣A的成分有C和Fe2O3填化学式)
(3)步骤②洗涤沉淀的方法是向漏斗中加水至浸没沉淀,待水自然流下后,再重复2-3次
(4)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三脚架.
Ⅰ.(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成为CaO•3MgO•4SiO2.
(2)高分子材料可以分成无机高分子材料和有机高分子材料.[AlFe(OH)nCl6-n]m属于无机高分子材料,是一种新型高效净水剂,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为+3.
Ⅱ.高纯二氧化硅可用来制造光纤.某稻壳灰的成分如下表:
| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.61 |

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物的种类最多有3类,其中SiO2为酸性氧化物(填氧化物的类别)
(2)滤渣A的成分有C和Fe2O3填化学式)
(3)步骤②洗涤沉淀的方法是向漏斗中加水至浸没沉淀,待水自然流下后,再重复2-3次
(4)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三脚架.
13.下列说法不正确的是( )
| A. | 12C和13C为不同核素 | B. | 金刚石和C60互为同素异形体 | ||
| C. | 1H2和2H2互为同位素 | D. | 氧原子(18O)的结构示意图为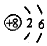 |
10.纯净的水呈中性,这是因为( )
| A. | 纯水中c(H+)=c(OH-) | B. | 纯水PH=7 | ||
| C. | 纯水的离子积KW=1.0×10-14 | D. | 纯水是非电解质 |
17.与100mL 0.5mol/L NaCl溶液中的Cl-的物质的量浓度相同的是( )
| A. | 100mL 0.5 mol/L MgCl2溶液 | B. | 200mL 0.25 mol/L KCl溶液 | ||
| C. | 100mL 0.5 mol/L HCl溶液 | D. | 100mL 0.5 mol/L NaClO溶液 |
14.下列有关物质应用的叙述中,正确的是( )
| A. | 氢氧化钠可用于治疗胃酸过多 | |
| B. | 福尔马林可以用于是食品防腐剂 | |
| C. | 水玻璃浸泡过的木材既能防腐又能耐火 | |
| D. | Si用于制造光导纤维 |

