��Ŀ����
C1��ѧ��ָ��һ��̼ԭ�ӵĻ�����(��CH4��CO��CO2 CH3OH��HCHO��)�����ϳɸ��ֻ�ѧƷ�ļ�������ú����Ȼ���ƺϳ����ٽ�һ���Ʊ����ֻ�����Ʒ�ͽྻȼ�ϣ��ѳ�Ϊ����ѧ��ҵ��չ�ı�Ȼ���ơ����м״���C1��ѧ�Ļ�����
��CO��H2��һ�������������Ҷ�������n(CO)/n(H2)�� ��(������)
��������ƽ�������CmHn��ʾ����ϳ�����Ӧ����n(CO)��n(H2)�� ��(��m �� n��ʾ)��
�ۼ״���һ����������CO��H2���������л���A��A�����Ӿۿ����ɸ߷���
 д������A�Ļ�ѧ����ʽ ��
д������A�Ļ�ѧ����ʽ ��
��![]() ��
��![]()
��2CO+H2+2CH3OH��CH3COOCH=CH2+H2O

��ϰ��ϵ�д�
�����Ŀ

����Ӧ����(ѹ��2.0~ 10.0 MPa���¶�230~ 280��)�������з�Ӧ��
CO(g)+2H2(g) CH3OH(g) ��H=-90.7 kJ/mol ��
CH3OH(g) ��H=-90.7 kJ/mol ��
2CH3OH(g) CH3OCH3(g)+H2O(g) ��H = -23.5 kJ/mol ��
CH3OCH3(g)+H2O(g) ��H = -23.5 kJ/mol ��
CO(g) +H2O(g) CO2(g)+H2(g) ��H=-41.2 kJ/mol ��
CO2(g)+H2(g) ��H=-41.2 kJ/mol ��
�ٴ���Ӧ�����ܷ�Ӧ3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)�ġ�H=_____��830�� ʱ��Ӧ�۵�K=1.0�����ڴ���Ӧ���з�Ӧ�۵�K_______���>������<����=����1.0��
CH3OCH3(g)+CO2(g)�ġ�H=_____��830�� ʱ��Ӧ�۵�K=1.0�����ڴ���Ӧ���з�Ӧ�۵�K_______���>������<����=����1.0��
�����������У�����ѭ��ʹ�õ�������____________��
CO(g)+2H2(g)
 CH3OH(g) ��H=-90.7 kJ/mol ��
CH3OH(g) ��H=-90.7 kJ/mol ��2CH3OH(g)
 CH3OCH3(g)+H2O(g) ��H = -23.5 kJ/mol ��
CH3OCH3(g)+H2O(g) ��H = -23.5 kJ/mol ��CO(g) +H2O(g)
 CO2(g)+H2(g) ��H=-41.2 kJ/mol ��
CO2(g)+H2(g) ��H=-41.2 kJ/mol �� �ٴ���Ӧ�����ܷ�Ӧ3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g)�ġ�H=_____��830�� ʱ��Ӧ�۵�K=1.0�����ڴ���Ӧ���з�Ӧ�۵�K_______���>������<����=����1.0��
CH3OCH3(g)+CO2(g)�ġ�H=_____��830�� ʱ��Ӧ�۵�K=1.0�����ڴ���Ӧ���з�Ӧ�۵�K_______���>������<����=����1.0�� �����������У�����ѭ��ʹ�õ�������____________��
 CO(g)+2H2(g) ��H=-35.6 kJ/mol���÷�Ӧ��_____����Է������Է�������Ӧ��
CO(g)+2H2(g) ��H=-35.6 kJ/mol���÷�Ӧ��_____����Է������Է�������Ӧ�� 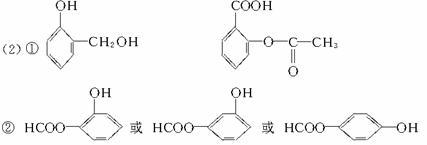 д������A�Ļ�ѧ����ʽ��_________________________________��
д������A�Ļ�ѧ����ʽ��_________________________________��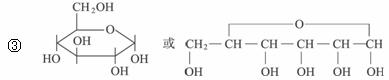
 (2)������ƽ�������CmHn��ʾ����ϳ�����Ӧ����n(CO)��n(H2)�� �� ��(��m �� n��ʾ)��
(2)������ƽ�������CmHn��ʾ����ϳ�����Ӧ����n(CO)��n(H2)�� �� ��(��m �� n��ʾ)��