题目内容
3.下列说法中正确的数目为( )①氢元素有三种核素H、D、T,HD属于化合物
②发生有效碰撞的分子一定是活化分子
③不同元素组成的多原子分子里的化学键一定是极性键
④12g NaHS04固体中含有的阴阳离子总数为0.3NA
⑤同主族元素原子序数可相差2、8、16、26、36、50等
⑥过渡元素即为所有副族元素,又叫过渡金属
⑦I2升华时破坏分子间作用力.
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
分析 ①同种元素组成的纯净物是单质;
②只有活化分子才可能发生有效碰撞;
③把握极性键是形成于不同种原子之间的共价键.
④NaHS04固体中只含钠离子和HSO4-.
⑤同主族元素的原子序数相差的是2、8、8、18、18、32、32这几个数字的一个或几个的连续的加和.
⑥过渡元素包括七个副族和一个第ⅤⅢ族.
⑦I2升华是物理变化,只破坏了分子间作用力.
解答 解:①单质是由同种元素组成的纯净物,而HD中的H和D都是氢原子,都属于氢元素,故是单质,故①错误;
②只有活化分子才可能发生有效碰撞,普通分子不能发生有效碰撞,故②正确;
③极性键是形成于不同种原子之间的共价键,故不同元素组成的多原子分子里的化学键一定含极性键,但不一定都是极性键,故③错误;
④NaHS04固体中只含钠离子和HSO4-,故12g NaHS04固体即0.1mol NaHS04中含0.2mol离子,即阴阳离子总数为0.2NA,故④错误;
⑤同主族元素的原子序数相差的是2、8、8、18、18、32、32这几个数字的一个或几个的连续的加和,故可相差2、8、16、26、36、50,故⑤正确;
⑥七个副族和一个第ⅤⅢ族合称过渡元素,故⑥错误;
⑦I2升华是物理变化,只破坏了分子间作用力,故⑦正确.
故正确的数目为3;
故选B.
点评 本题考查了单质化合物的概念、极性键的形成、过渡元素的范围等等内容,考查范围广,综合性强,难度适中.

练习册系列答案
相关题目
13.同一主族的两种元素的核外电子差值不可能为( )
| A. | 2 | B. | 8 | C. | 18 | D. | 30 |
18.向下列液体中滴加稀硫酸,生成沉淀,继续滴加稀硫酸,沉淀又溶解的是( )
| A. | Na2CO3溶液 | B. | BaCl2溶液 | C. | Ba(OH)2溶液 | D. | Fe(OH)3胶体 |
8.下列各项操作中,发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向Ca(ClO)2溶液中通入过量CO2 ②向AlCl3溶液中逐滴加入过量氨水
③向AgNO3溶液中逐滴加入过量氨水 ④向Na2SiO3溶液中逐滴加入过量的盐酸.
①向Ca(ClO)2溶液中通入过量CO2 ②向AlCl3溶液中逐滴加入过量氨水
③向AgNO3溶液中逐滴加入过量氨水 ④向Na2SiO3溶液中逐滴加入过量的盐酸.
| A. | 只有②③ | B. | 只有①③ | C. | 只有①②③ | D. | ①②③④ |
12.在溶液中加入足量的Na2O2后仍能大量共存的离子组是( )
| A. | Na+、Fe2+、Cl-、SO42- | B. | K+、[Al(OH)4]-、Cl-、SO42- | ||
| C. | Ca2+、Mg2+、NO3-、HCO${\;}_{3}^{-}$ | D. | Na+、Cl-、CO32-、SO32- |
11.以下各组物质既不是同系物也不是同分异构体的是( )
| A. | CH4和C10 H22 | B. | 1-己烯和环己烷 | C. | C2H4和1-丁烯 | D. | 乙二醇和丙三醇 |
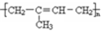 )为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.
)为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.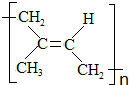 .
.