题目内容
完成下列离子方程式(给出物质的计量数不能改变)
(1) +2 + +2 ═BaSO4↓+2H2O
(2) +Ca2++ ═CaCO3↓+
(3)Cu2++ +Ba2++ ═BaSO4↓+Cu(OH)2↓
(4) +3H+═Fe3++ .
(1)
(2)
(3)Cu2++
(4)
考点:离子方程式的书写
专题:离子反应专题
分析:(1)生成硫酸钡和水,则该离子反应为钡离子、硫酸根离子、氢离子和氢氧根离子的反应;
(2)生成碳酸钙,离子反应可能为碳酸氢根离子、钙离子、氢氧根离子的反应;
(3)生成硫酸钡和氢氧化铜,则为氢氧化钡和硫酸铜的离子反应;
(4)与酸反应生成铁离子,应为氢氧化铁和非氧化性酸生成铁离子和水.
(2)生成碳酸钙,离子反应可能为碳酸氢根离子、钙离子、氢氧根离子的反应;
(3)生成硫酸钡和氢氧化铜,则为氢氧化钡和硫酸铜的离子反应;
(4)与酸反应生成铁离子,应为氢氧化铁和非氧化性酸生成铁离子和水.
解答:
解:(1)生成硫酸钡和水,则该离子反应为钡离子、硫酸根离子、氢离子和氢氧根离子的反应,离子反应为Ba2++2H++SO42-+2OH-═BaSO4↓+2H2O,
故答案为:Ba2+;H+;SO42-;OH-;
(2)生成碳酸钙,离子反应可能为碳酸氢根离子、钙离子、氢氧根离子的反应,离子反应为HCO3-+Ca2++OH-═CaCO3↓+H2O,
故答案为:HCO3-;OH-;H2O;
(3)生成硫酸钡和氢氧化铜,则为氢氧化钡和硫酸铜的离子反应,离子反应为Cu2++SO42-+Ba2++2OH-═BaSO4↓+Cu(OH)2↓,故答案为:SO42-;2OH-;
(4)与酸反应生成铁离子,应为氢氧化铁和非氧化性酸生成铁离子和水,离子反应为Fe(OH)3+3H+═Fe3++3H2O,故答案为:Fe(OH)3;3H2O.
故答案为:Ba2+;H+;SO42-;OH-;
(2)生成碳酸钙,离子反应可能为碳酸氢根离子、钙离子、氢氧根离子的反应,离子反应为HCO3-+Ca2++OH-═CaCO3↓+H2O,
故答案为:HCO3-;OH-;H2O;
(3)生成硫酸钡和氢氧化铜,则为氢氧化钡和硫酸铜的离子反应,离子反应为Cu2++SO42-+Ba2++2OH-═BaSO4↓+Cu(OH)2↓,故答案为:SO42-;2OH-;
(4)与酸反应生成铁离子,应为氢氧化铁和非氧化性酸生成铁离子和水,离子反应为Fe(OH)3+3H+═Fe3++3H2O,故答案为:Fe(OH)3;3H2O.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应及配平的考查,注意离子反应中保留化学式的物质、逆向思维法的应用、原子守恒等,综合性较强,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应的离子方程式正确的是( )
| A、硫酸铝溶液和小苏打溶液反应:Al3++3HCO3-═3CO2↑+Al(OH)3↓ |
| B、向Ca(ClO)2溶液中通入二氧化硫:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| C、硫化亚铁中加入盐酸:S2-+2H+═H2S↑ |
| D、钠和冷水反应:Na+2H2O═Na++H2↑+2OH- |
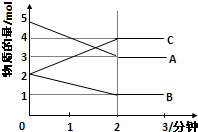 某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.则该反应的反应物是
某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.则该反应的反应物是