��Ŀ����
��֪��SO2+
| 1 |
| 2 |
��1����T1�¶�ʱ���÷�Ӧ��ƽ�ⳣ��K=
| 10 |
| 3 |
��2����T2�¶�ʱ����ʼ��100L���ܱ������м���4.0molSO2��10.0molO2��һ�������µ���Ӧ�ﵽƽ��ʱ���ų�����196kJ����ʱ���������ת����Ϊ______��
��3���ڣ�2���еķ�Ӧ�ﵽƽ��ı�������������ʹSO2ƽ��Ũ�ȱ�ԭ����С����______������ĸ����
A�������¶Ⱥ�����������䣬����1.0molO2
B�������¶Ⱥ�������ѹǿ���䣬����2.0molSO2��5.0molO2
C�������¶�
D����������������ʱ����С�������ݻ�
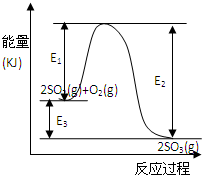
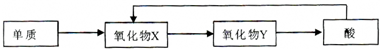
��4��������������ͼ��ʾװ���õ绯ѧԭ���������ᣬд��ͨ��SO2�ĵ缫�ĵ缫��Ӧʽ��______��
��5����������Ƶ������Σ���һ���¶��£���K2SO4��Һ�еμ�Na2CO3��Һ��BaCl2��Һ�������ֳ�������ʱ��
c(C
| ||
c(S
|

| 1 |
| 2 |
��ΪŨ����QC=
| c(SO3) | ||
c(SO2)[c(O2)]
|
| ||||||
|
��2����T2�¶�ʱ����ʼ��100L���ܱ������м���4.0molSO2��10.0molO2��һ�������µ���Ӧ�ﵽƽ��ʱ���ų�����196kJ����1molSO2��ȫ��Ӧ����98KJ����һ�������µ���Ӧ�ﵽƽ��ʱ���ų�����196kJ�����Ķ����������ʵ���=
| 1mol��196KJ |
| 98KJ |
SO2��g��+
| 1 |
| 2 |
��ʼ����mol�� 4 10 0
�仯����mol�� 2 1 2
ƽ������mol�� 2 9 2
����SO2��ת���ʦ�=
| 2mol |
| 4mol |
��3��A�������¶Ⱥ�����������䣬O2��Ũ������ƽ�������ƶ���SO2��Ũ�ȼ�С������A��ȷ��
B�������¶Ⱥ�������ѹǿ���䣬����2.0molSO2��5.0molO2���µ�ƽ����ԭƽ���Ч��SO2��Ũ�Ȳ��䣬����B����
C�������¶ȣ�ƽ������ȵķ����ƶ���������ӦΪ���ȣ�����ƽ�������ƶ���SO2��Ũ�ȼ�С������C��ȷ��
D����������������ʱ����С�������ݻ���SO2��Ũ��˲������֮��ƽ��������������ٵķ����ƶ�����������Ӧ�����ƶ���SO2��Ũ�ȼ�С���ٴε���ƽ��ʱSO2��Ũ���Ա�ԭ��������D����
�ʴ�Ϊ��A��C��
��4������ͼװ�÷�������������ʧ���ӷ���������Ӧ��������������Ϊ������������ˮ��������缫��ӦΪ��SO2+2H2O=SO42-+4H++2e-��
�ʴ�Ϊ��SO2+2H2O=SO42-+4H++2e-��
��5����һ���¶��£���K2SO4��Һ�еμ�Na2CO3��Һ��BaCl2��Һ�������ֳ�������ʱ�������ܶȻ�������֪���������ᱵ��������ת����BaCO3+SO42-=BaSO4+CO32-�����̼�ᱵ�����ᱵ�ܶȻ�������
| c(CO22-) |
| c(SO42-) |
| Ksp(BaCO3) |
| Ksp(BaSO4) |
| 5.2��10-9 |
| 1.3��10-10 |
�ʴ�Ϊ��40��

 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д���1����֪1.0mol��L��1NaHSO3��Һ��pHΪ3.5�������Һ����Ũ�ȴӴ�С��˳��Ϊ �������ӷ��ű�ʾ����
 ��2����֤��Na2SO3��Һ�д���ˮ��ƽ��SO32��+H2O
��2����֤��Na2SO3��Һ�д���ˮ��ƽ��SO32��+H2O![]() HSO3��+OH������ʵ�� ������ţ���
HSO3��+OH������ʵ�� ������ţ���
A�������̪��Һ��죬�ټ���H2SO4��Һ��ɫ��ȥ
B�������̪��Һ��죬�ټ�����ˮ���ɫ��ȥ
C�������̪��Һ��죬�ڼ���BaCl2��Һ����������Һ�ɫ��ȥ
��3����ҵ�����ô�������Ӧ��SO2ת��ΪSO3��2SO2+ O2 ![]() 2SO3����ij�¶��£��˷�Ӧ����ʼŨ��c��SO2��=1.0mol��L��1��c��O2��=1.5mol��L��1���ﵽƽ���SO2��ת����Ϊ50%������¶��¸÷�Ӧ��ƽ�ⳣ��K�� ��
2SO3����ij�¶��£��˷�Ӧ����ʼŨ��c��SO2��=1.0mol��L��1��c��O2��=1.5mol��L��1���ﵽƽ���SO2��ת����Ϊ50%������¶��¸÷�Ӧ��ƽ�ⳣ��K�� ��
��4����������Һ�У������(KIO3)���������ƿɷ������·�Ӧ��
2IO3����5SO32����2H��===I2��5SO42����H2O
���ɵĵ�����õ�����Һ���飬���ݷ�Ӧ��Һ������ɫ�����ʱ���������÷�Ӧ�����ʡ�ijͬѧ���ʵ�����±���ʾ��
| 0.01mol��L��1 KIO3 ������Һ(������)�����/mL | 0.01mol��L��1 Na2SO3 ��Һ�����/mL | H2O����� /mL | ʵ�� �¶� /�� | ��Һ������ɫʱ����ʱ��/s | |
| ʵ��1 | 5 | V1 | 35 | 25 | |
| ʵ��2 | 5 | 5 | 40 | 25 | |
| ʵ��3 | 5 | 5 | V2 | 0 |
����V2=___________mL����ʵ���Ŀ����______________ ______��
 ���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮T��ʱ��Ӧ2SO2��g��+O2��g��?2SO3��g�������е������仯��ͼ��ʾ���ش��������⣮
���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮T��ʱ��Ӧ2SO2��g��+O2��g��?2SO3��g�������е������仯��ͼ��ʾ���ش��������⣮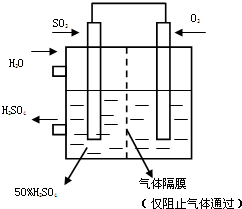

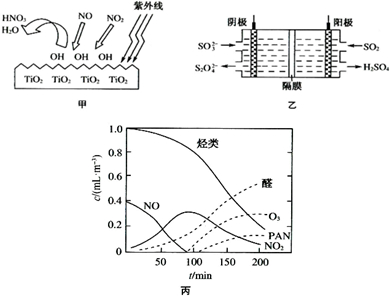
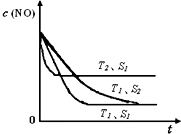 ���������Ǵ�����Ⱦ��֮һ��������������ķ����ж��֣�
���������Ǵ�����Ⱦ��֮һ��������������ķ����ж��֣�