题目内容
反应Fe2O3(s)+3CO(g)
2Fe(s)+3CO2(g)在一容积可变的密闭容器中进行,试回答:
(1)增加Fe的量,其反应速率 (填“加快”、“不变”或“减慢”,下同).
(2)将容器的体积缩小一半,其反应速率 .
(3)保持体积不变,充入Ne使体系压强增大,其正反应速率 .
(4)保持压强不变,充入Ne使容器的体积增大,其正反应速率 .
| ||
(1)增加Fe的量,其反应速率
(2)将容器的体积缩小一半,其反应速率
(3)保持体积不变,充入Ne使体系压强增大,其正反应速率
(4)保持压强不变,充入Ne使容器的体积增大,其正反应速率
考点:化学平衡的影响因素
专题:化学平衡专题
分析:(1)改变纯固体的量,对反应速率无影响;
(2)将容器的体积缩小一半,气体的浓度变大,反应速率加快;
(3)保持体积不变,充入N2使体系压强增大,反应体系中各物质的浓度不变;
(4)保持压强不变,充入N2使容器的体积增大,反应体系中气体的浓度减小.
(2)将容器的体积缩小一半,气体的浓度变大,反应速率加快;
(3)保持体积不变,充入N2使体系压强增大,反应体系中各物质的浓度不变;
(4)保持压强不变,充入N2使容器的体积增大,反应体系中气体的浓度减小.
解答:
解:(1)改变纯固体的量,对反应速率无影响,则增加Fe的量,其正反应速率不变,故答案为:不变;
(2)将容器的体积缩小一半,气体的浓度变大,反应速率加快,则正逆反应速率均加快,故答案为:加快;
(3)保持体积不变,充入Ne使体系压强增大,反应体系中各物质的浓度不变,则正逆反应速率不变,故答案为:不变;
(4)保持压强不变,充入Ne使容器的体积增大,反应体系中气体的浓度减小,则正反应速率减慢,故答案为:减慢.
(2)将容器的体积缩小一半,气体的浓度变大,反应速率加快,则正逆反应速率均加快,故答案为:加快;
(3)保持体积不变,充入Ne使体系压强增大,反应体系中各物质的浓度不变,则正逆反应速率不变,故答案为:不变;
(4)保持压强不变,充入Ne使容器的体积增大,反应体系中气体的浓度减小,则正反应速率减慢,故答案为:减慢.
点评:本题考查化学反应速率的影响因素的分析判断,综合性较强,注重对常考查点的考查,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
下列叙述与电化学腐蚀有关的是( )
| A、切过菜的菜刀不及时清洗易生锈 |
| B、在空气中金属镁、铝都具有较好的抗腐蚀性 |
| C、红热的铁丝与水接触时,表面形成了蓝黑色的物质 |
| D、把铁片投入到氯化铜的溶液中,在铁表面上附着一层红色的铜 |
在淀粉碘化钾溶液中加入少量NaClO溶液,振荡,溶液变蓝.在上述溶液中加入足量的Na2SO3溶液,蓝色逐渐消失.下列判断错误的是( )
| A、氧化性:ClO->I2 |
| B、蓝色逐渐消失说明Na2SO3具有漂白性 |
| C、漂白粉溶液可使淀粉碘化钾试纸变蓝 |
| D、向新制氯水中加入足量亚硫酸钠溶液,氯水褪色 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、5.6g铁粉在2.24L(标准状况)氯气中充分燃烧,失去的电子数为0.3NA |
| B、常温下,1 mol CO2和O2的混合气体中所含氧原子数为2NA |
| C、3.2g Cu与10.0g 98%的H2SO4充分反应可得0.05 NA个SO2气体分子 |
| D、电解精炼铜时每转移NA个电子,阳极上溶解的铜的质量一定为32g |
某酸式盐NaHY的水溶液显碱性,下列叙述正确的是( )
| A、H2Y的电离方程式:H2Y?2H++Y2- |
| B、HY-的水解方程式:HY-+H2O?H3O++Y2- |
| C、该酸式盐溶液中离子浓度关系:c(Na+)>c(HY-)>c(OH-)>c(H+) |
| D、该酸式盐溶液中离子浓度关系:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) |
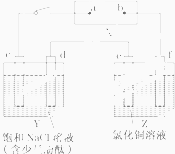 如图X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.
如图X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.